Die Sequenzierung des humanen Genoms und die Identifizierung von etwa 90 Proteinen mit Tyrosinkinase-Domäne sind ein wichtiger Fortschritt für die Entwicklung gezielter molekularer Therapieansätze bei Tumorerkrankungen (1). Über die erfolgreiche Therapie der chronischen myeloischen Leukämie mit Imatinib (Glivec®) haben wir wiederholt berichtet (2-4). Bei dieser Erkrankung reicht vermutlich die unkontrollierte Tyrosinkinaseaktivität von BCR-ABL für die Leukämieentstehung aus. Sie ist somit eine ideale therapeutische Zielstruktur für Imatinib, einen Inhibitor dieser Tyrosinkinase. Demgegenüber sind die bisher bekannten Ergebnisse mit Therapiestrategien, die bei soliden Tumoren gegen den „Epidermal Growth Factor Receptor” (EGFR) bzw. EGFR-assoziierte Signalwege gerichtet sind, eher enttäuschend (5-7). Mit neuen, sehr teuren Wirkstoffen wie Gefitinib oder Cetuximab konnten in größeren Studien nur Ansprechraten von 10-20% bei Patienten mit nicht-kleinzelligem Bronchialkarzinom bzw. metastasiertem kolorektalem Karzinom erreicht werden (7). Zellbiologische Erkenntnisse über die Korrelation zwischen z.B. somatischen Mutationen des EGFR bzw. Aktivierung der in Tumorzellen häufig gestörten Signaltransduktionswege und dem therapeutischen Ansprechen auf monoklonale Antikörper gegen den EGFR oder auf Inhibitoren von Tyrosinkinasen sind deshalb sehr wichtig, um solche Patienten besser und frühzeitiger zu erkennen, die von derartigen innovativen Therapiestrategien tatsächlich profitieren (8).
Vor diesem Hintergrund sind die Ergebnisse klinischer Phase-II-Studien mit Cetuximab, einem monoklonalen Antikörper gegen EGFR, bei Patienten mit Irinotecan-refraktären metastasierten kolorektalen Karzinomen zu interpretieren. In einer offenen, multizentrischen unkontrollierten Phase-II-Studie wurde bei Patienten mit Chemotherapie-refraktären kolorektalen Karzinomen und Expression des EGFR auf den Tumorzellen die antitumoröse Aktivität und Toxizität einer Monotherapie mit Cetuximab untersucht (9). Alle Patienten hatten zuvor Irinotecan (Campto®; 10) entweder allein oder im Rahmen einer Kombinationschemotherapie erhalten und auf diese Therapie nicht mehr angesprochen. Cetuximab wurde wöchentlich als intravenöse Kurzinfusion verabreicht (400 mg/m2 bei der ersten Applikation, 250 mg/m2 bei den folgenden Applikationen). Insgesamt wurden 57 Patienten behandelt, von denen nur fünf Patienten ein partielles Ansprechen und 21 Patienten eine stabile Erkrankung zeigten. Unerwünschte Arzneimittelwirkungen (UAW) waren vorwiegend Hautreaktionen (akneiforme Hautveränderungen) und unspezifische Symptome, wie körperliche Schwäche, Abgeschlagenheit oder Lethargie.
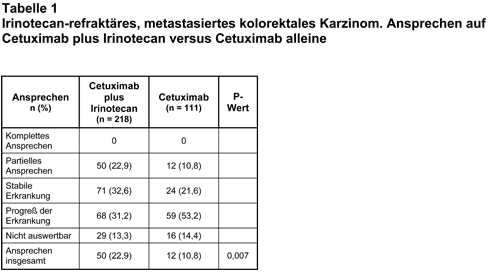
Im Juli 2004 wurden die vollständigen Ergebnisse einer von Merck finanziell unterstützten, inhaltlich konzipierten und medizinisch bzw. statistisch ausgewerteten europäischen randomisierten, multizentrischen Studie publiziert (11). Patienten mit EGFR-positiven, Irinotecan-refraktären metastasierten kolorektalen Karzinomen wurden entweder mit der Kombination von Irinotecan plus Cetuximab oder nur mit Cetuximab behandelt. Auf das Design dieser Studie, das untersuchte Patientenkollektiv, primäre bzw. sekundäre Endpunkte, Ergebnisse und UAW sind wir bereits ausführlich eingegangen (6). Die wesentlichen Ergebnisse sind in Tab. 1 zusammengefaßt. Sie verdeutlichen, daß sich die Ansprechrate und die mediane Zeit bis zum Progreß der Erkrankung signifikant zugunsten der mit der Kombinationstherapie behandelten Gruppe unterscheiden. Ein Unterschied im medianen Überleben ergab sich jedoch nicht. Cetuximab (Erbitux®) wurde am 30. Juni 2004 von der europäischen Arzneimittelagentur (EMEA) zur Behandlung von Patienten mit EGFR-exprimierendem, metastasiertem kolorektalem Karzinom in Kombination mit Irinotecan zugelassen, die zuvor auf eine Chemotherapie mit Irinotecan nicht mehr angesprochen haben. Diese rasche Zulassung wirft zahlreiche Fragen auf. Angesichts der fehlenden Korrelation zwischen der Expression von EGFR in den Tumorzellen und dem klinischen Ansprechen stellt sich das Problem, ob möglicherweise Mutationen im EGFR bzw. Aktivierung spezieller „Downstream”-Signaltransduktionswege zu einer besseren Identifizierung der von Cetuximab profitierenden Patienten führen können. Leider liegen hierzu bisher keine aussagekräftigen wissenschaftlichen Ergebnisse vor. Die von DakoCytomation in Zusammenarbeit mit Merck propagierte Diagnostik des EGFR-Status anhand eines immunhistochemischen Tests mag zwar als Einschlußkriterium für klinische Studien geeignet sein, verteuert jedoch die Therapie und ist nicht geeignet, das Ansprechen auf Cetuximab vorherzusagen. Auch sind die Gründe für das bessere Ansprechen von Patienten mit deutlichen Hautreaktionen bisher unklar. Ob die von den Autoren der Studie diskutierte individualisierte Dosistitration von Cetuximab, basierend auf dem Auftreten bzw. dem Schweregrad der Hautveränderungen, geeignet ist, die Wirksamkeit zu verbessern, erscheint sehr fraglich.
Zu der Studie von D. Cunningham et al. sind im N. Engl. J. Med. zwei sehr lesenswerte Editorials erschienen, in denen die Kosten neuer Wirkstoffe zur Behandlung kolorektaler Karzinome kritisch diskutiert und die Schwächen dieser als randomisierte Phase-II-, aber nicht als Phase-III-Studie zu bezeichnenden klinischen Prüfung dargestellt werden (12, 13).
Fazit: Cetuximab ist ein neuer chimärer monoklonaler IgG1-Antikörper, der gegen den epidermalen Wachstumsfaktor-Rezeptor (EGFR) gerichtet ist. Die Wirksamkeit von Cetuximab in der Behandlung von Patienten mit Chemotherapie-refraktärem kolorektalem Karzinom als Monotherapie ist gering (Ansprechraten um 10%). Auch in der Kombination mit Irinotecan werden nur Ansprechraten von 23% bzw. eine Verlängerung der medianen Zeit bis zum Progreß der Erkrankung von 2,6 Monaten, nicht aber eine signifikante Verlängerung des medianen Überlebens durch Cetuximab erreicht. Zukünftige Studien müssen sich verstärkt mit molekularen Parametern befassen, mit denen valide und frühzeitig die Patienten identifiziert werden können, die auf Cetuximab ansprechen. Die Indikation für Cetuximab außerhalb klinischer Studien sollte aufgrund der geringen Wirksamkeit und der sehr hohen Kosten (bei einer Körperoberfläche von 1,8 m2 ca. 31320 EUR für eine Monotherapie und ca. 50088 EUR für die Kombination mit Irinotecan über 24 Wochen) sehr kritisch geprüft und Alternativen überlegt werden. Der Stellenwert von Cetuximab in Kombination mit Irinotecan oder 5-FU bzw. Oxaliplatin-haltigen Therapiestrategien in der primären Therapie metastasierter kolorektaler Karzinome ist unklar.
Literatur
- Baselga, J., und Arribas, J.: Nat. Med. 2004, 10, 786.
- AMB 2001, 35, 47b.
- AMB 2003, 37, 28.
- AMB 2003, 37, 78.
- AMB 2003, 37, 23.
- AMB 2004, 38, 31.
- AMB 2004, 38, 53.
- Cappuzzo, F., et al.: J. Natl. Cancer. Inst. 2004, 96, 1133.
- Saltz, L.B., et al.: J. Clin. Oncol. 2004, 22, 1201.
- AMB 2002, 36, 3.
- Cunningham, D., et al.: N. Engl. J. Med. 2004, 351, 337.
- Schrag, D.: N. Engl. J. Med. 2004, 351, 317.
- Erlichman, C., und Sargent, D.J.: N. Engl. J. Med. 2004, 351, 391.