Unter sekundärer Wundheilung versteht man einen langwierigen Heilungsprozess großflächiger oder kontaminierter Wunden, bei dem Granulationsgewebe von den Wundrändern und aus der Tiefe wachsend die Wunde schrittweise verschließt. Dieser Prozess dauert oft mehrere Monate und schränkt die Lebensqualität erheblich ein. Derartige Wunden an den Füßen oder Unterschenkeln brauchen für die Heilung fast doppelt so lange wie an anderen Körperstellen [1].
Übliche Wundauflagen sind Gaze, Hydrokolloide oder Alginate. Sie müssen oft mehrmals am Tag gewechselt werden und sind teuer (Apothekeneinkaufspreis pro Stück zwischen 2-130 €; Übersicht bei [2]). Alternativ oder bei Versagen dieser Therapie kann eine Vakuumversiegelungstherapie (VAC) durchgeführt werden: Eine spezielle schwammartige Wundauflage wird unter Folienabdeckung in einem geschlossenen System mit einer Pumpe kombiniert, die mittels Unterdruck Wundsekret aufsaugen kann [3]; dies soll Wundinfektionen und Wundödeme reduzieren, die Durchblutung sowie Granulation der Wunde fördern und eine Grundlage schaffen für eine möglicherweise erforderlich werdende plastische Deckung. Die Hersteller versprechen eine schnellere Heilung [4].
Die VAC zum sekundären Wundverschluss wurde in Deutschland 2020 als neue Gebührenordnungsposition aufgenommen. Die Kostenpauschalen für die Verbrauchsmaterialien wurden in Deutschland gerade wegen stark steigender Materialpreise erhöht: Bei Wundflächen mit einer Größe von bis zu 20 cm2 von 65,49 auf 91,14 € und für größere Wunden von 71,39 auf 94,27 € [5].
Die VAC wurde in den letzten Jahren intensiv eingesetzt, obwohl sie teuer ist und es keine verlässlichen Daten gibt, die den klinischen Nutzen oder eine Kosteneffizienz belegen ([6], [7], [8], [9]). Ein systematisches Cochrane-Review [3] fand nur 2 Studien zur VAC ([6], [10]) mit Hinweisen auf eine schnellere Heilung; sie waren aber klein und mit einem erhöhten Risiko für systemische Fehler (Bias) behaftet.
Nach einer 5 Jahre alten Metaanalyse mit 48 Studien scheint eine VAC insgesamt für die Wundheilung vorteilhaft zu sein im Vergleich zu einer Standardtherapie (ST); bzgl. Infektion, Amputation, Schmerzen und Lebensqualität wurde aber kein Unterschied gefunden [11]. Auch diese Studien waren von geringer Qualität und hatten ein hohes Risiko für Verzerrung.
Der Gemeinsame Bundesausschuss (G-BA) hatte 2019 den Nutzen und die Wirtschaftlichkeit der VAC nach Studienlage insgesamt positiv bewertet; spezielle Nachteile fanden sich nicht [12].
In einer offenen Studie an 28 Kliniken in Großbritannien sollten bestehende Unsicherheiten beseitigt und eine mögliche Überlegenheit der VAC gegenüber der ST geprüft werden [13]. Die Studie wurde aus öffentlichen Mitteln finanziert und ist die erste multizentrische, randomisierte, kontrollierte Studie zur VAC im Vergleich zu einer ST.
Studiendesign: Von 2019 bis 2023 wurden Personen eingeschlossen mit einer schlecht heilenden Wunde jedweder Lokalisation und nach einer höchstens 6 Wochen zurückliegenden Operation. Die Wundfläche musste > 80% vitales Gewebe aufweisen und keine Indikation für ein chirurgisches Debridement haben. Ausschlusskriterien waren u.a. ein hohes Blutungsrisiko, akute systemische Infektionen und chronische Wunden.
Die Teilnehmenden wurden nach dem Zufallsprinzip offen 1:1 randomisiert in eine VAC oder ST. Während der COVID-19-Pandemie war die laufende Überprüfung von März 2020 bis Januar 2024 auf wöchentliche Telefonate reduziert. Eine Wundheilung (vollständige Epithelisierung ohne Kruste) wurde umgehend durch Fotos dokumentiert und die Konstanz des Heilungsprozesses eine und zwei Wochen später erneut geprüft. Die Auswertung der Fotos wurde von erfahrenen, unabhängigen Beobachtern ohne Kenntnis der Therapie durchgeführt. Die Wunden wurden je nach Lokalisation (Fuß und Knöchel, Bein, Bauch oder andere) und der Wundfläche (< 28 cm² oder ≥ 28 cm²) kategorisiert und die Teilnehmer 12 Monate lang nachbeobachtet.
In Fragebögen wurden Scores erfasst zur Wundinfektion („Bluebelle Wound Healing Questionnaire“ = WHQ; [14]), zu Wundschmerzen über die visuelle Analogskala = VAS (0 keine Schmerzen, 100 die schlimmsten vorstellbaren Schmerzen) jeweils zu Studienbeginn und 3 Monate später sowie Scores zu gesundheitsbezogener Lebensqualität (EQ-5D-5L; [15]) bzw. zu wundbezogenen ärztlichen Konsultationen jeweils nach 3, 6 und 12 Monaten.
Primärer Studienendpunkt war die vollständige Wundheilung. Sekundäre Endpunkte waren Wundinfektion, Behandlung mit Antibiotika, Krankenhauseinweisung oder -entlassung, operative Wundrevision, Amputation bzw. Tod innerhalb von 12 Monaten, die ermittelte Heilungszeit lt. Fotodokumentation und unerwünschte Ereignisse, die über die zu erwartenden (leichte Wundinfektion, Zellulitis, Ödem oder Mazeration) hinausgingen.
Ergebnisse: Von Mai 2019 bis Januar 2023 wurden 1.895 Patienten mit einer schlecht heilenden Wunde evaluiert, von denen jedoch nur 686 (36,2%) die Einschlusskriterien erfüllten und einwilligten. Das mediane Alter betrug 63 Jahre, 75% waren Männer. Fast alle hatten eine einzelne Wunde (n = 622; 90,7%), meistens nach einer Gefäßoperation (n = 619; 90,2%) und überwiegend am Fuß oder Bein (n = 620; 90,4%); 80% waren Diabetiker (n = 549). Die meisten Wunden waren verunreinigt; gut 30% hatten sehr große Wundflächen ≥ 28 cm2. Mit einer VAC wurden 349 und mit ST 337 behandelt.
Während der 12-monatigen Nachbeobachtung heilten die Wunden in beiden Gruppen bei knapp 60% vollständig ab: unter VAC bei 57,9% (n =202) und unter ST bei 58,2% (n = 196). Wegen Tod, Amputation, Studienabbruch oder Verlust konnten 159 Patienten (23,2%) nicht ausgewertet werden (83 unter VAC, 76 unter ST). Alle Daten gingen in die „Intention-to-Treat“-Analyse ein.
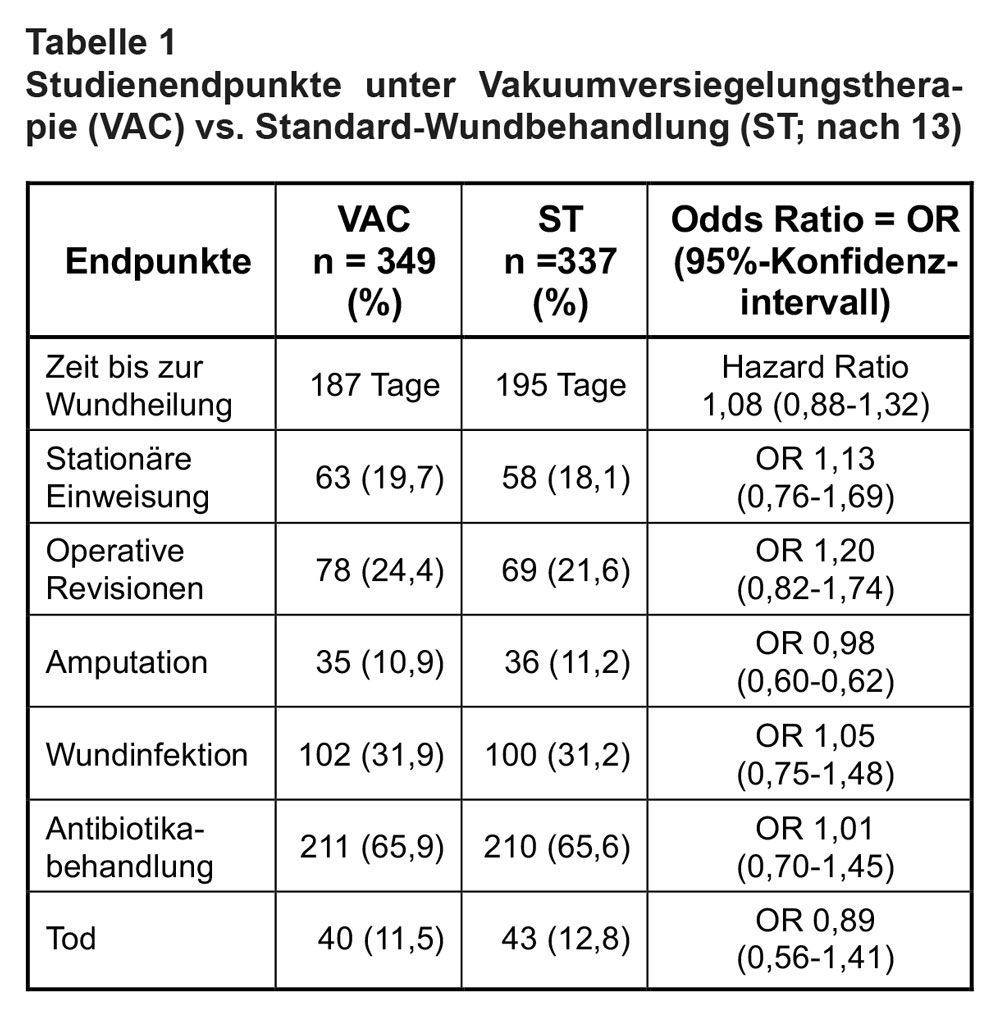
Die mediane Zeit bis zur Heilung betrug mit VAC 187 Tage und mit ST 195 Tage (Hazard Ratio = HR: 1,08; 95%-Konfidenzintervall = KI: 0,88-1,32; p = 0,47). Auch für die sekundären Endpunkte fanden sich keine signifikanten Unterschiede (s. Tab. 1).
Die ermittelten Scores zu Infektionszeichen, Schmerzen und Lebensqualität waren in beiden Gruppen fast gleich häufig: 150 unerwünschte Ereignisse bei 349 Patienten unter VAC (43,0%) vs. 139 bei 337 (41,2%) unter ST, meist Wundinfektionen. Als „schwerwiegend“ eingestufte unerwünschte Ereignisse gab es 9 unter VAC vs. 5 unter ST.
Eine Analyse zur Wirtschaftlichkeit errechnete für beide Therapien ähnlich hohe mittlere Behandlungskosten: für VAC wurden durchschnittliche Kosten von 5.782 £ (6.891 €; Spanne von ca. 5.000 bis 8.800 €) errechnet vs. 5.802 £ (6.915 €; Spanne 4.645 bis 9.185 €) unter ST. Der EQ-5D-5L-Score wurde zur Ermittlung der gesundheitsbezogenen Lebensqualität herangezogen. Ein qualitätskorrigiertes Lebensjahr („Quality-Adjusted Life Year“ = QALY) ist ein Maß für die Effektivität einer Behandlung auf einer Skala von 0 bis 1. QALY 1 entspricht einem Jahr in voller Gesundheit, QALY 0 dagegen Tod. Für die VAC wurde eine mittlere QALY von 0,581 (KI: 0,549-0,612) errechnet, für die ST 0,562 (0,528-0,595).
Diskussion: Es haben überwiegend Patienten mit schlecht heilenden Wunden der unteren Extremität teilgenommen, die meisten davon nach Gefäß-Operationen bei Diabetes mellitus. Die Studie ergab eine geringfügige, statistisch nicht signifikante Verkürzung (8 Tage) der Heilungszeit unter VAC im Vergleich zur ST über eine Nachbeobachtungszeit von 12 Monaten.
Die Kosten-Nutzen-Analyse und die zur Lebensqualität ergaben keinen statistisch signifikanten Vorteil für die VAC. Die Autoren geben zu bedenken, dass nur Wunden der unteren Extremität untersucht wurden, überwiegend bei Diabetes-assoziierten Wundheilungsstörungen, und dass auch in dieser sorgfältigen Studie eine Verzerrung durch fehlende Daten möglich sei. Auf andere sekundär heilende Wunden wie Steißbeinfistel, gefäßbedingte Wunden in der Leiste sowie venöse Ulzera oder Druckgeschwüre können die Ergebnisse nicht übertragen werden. Wunden mit viel Exsudation könnten von einer VAC möglicherweise stärker profitieren.
Diese Auffassung wird auch als Expertenmeinung in der 2023 überarbeiteten S3-Leitlinie zur Wundversorgung vertreten [16]. Es wurde nur eine „Kann-Empfehlung“ für den Einsatz ausgesprochen mit Bedenken beim Einsatz im ambulanten Bereich. Bei unvorhergesehenen technischen Problemen z.B. mit der Abdichtung durch die Folien oder mangelhaftem Sog könne es zur Retention von Exsudat mit Mazeration und Wundinfektion kommen.
Fazit
Eine große randomisierte, kontrollierte Studie aus Großbritannien konnte keine Überlegenheit einer Vakuumversiegelungstherapie (VAC) gegenüber einer konservativen Wundbehandlung bei Patienten mit überwiegend postoperativen und meistens diabetischen Wundheilungsstörungen an der unteren Extremität belegen. Die VAC war auch nicht kosteneffizienter, und die Zeit bis zur Wundheilung sowie die Scores zur gesundheitsbezogenen Lebensqualität waren etwa gleich. Eine VAC sollte daher nicht als Erstlinienbehandlung in Betracht gezogen werden. Offen bleibt, ob andere Wunden und solche mit starker Exsudation möglicherweise doch mehr von einer VAC profitieren könnten.
Literatur
- https://doi.org/10.1016/j.ijnurstu.2018.09.011 (Link zur Quelle)
- https://www.aok.de/gp/fileadmin/user_upload/Arzt_Praxis/Wirtschaftliche_Verordnung/nw_preisuebersichten_verbandstoffe.pdf (Link zur Quelle)
- Dumville, J.C., et al.: Cochrane Database Syst. Rev. 2015, 2015, CD011278. (Link zur Quelle)
- 3M. 3M Negative Pressure Wound Therapy (NPWT). (Link zur Quelle)
- https://www.kbv.de/html/1150_74278.php (Link zur Quelle)
- Chetter, I.C., et al.: Int. J. Nurs. Stud. 2019, 89, 62. (Link zur Quelle)
- Monsen, C., et al.: J. Vasc. Surg. 2014, 59, 145. (Link zur Quelle)
- Armstrong, D.G., Lavery, L.A.: Lancet 2005, 366, 1704. (Link zur Quelle)
- Dalla-Paola, L., et al.: J. Diabet. Foot Complications 2010, 2, 33. Zitiert nach: (Link zur Quelle)
- Biter, L.U., et al.: Dis. Colon Rectum 2014, 57, 1406. (Link zur Quelle)
- Zens, Y., et al.: Syst. Rev. 2020, 9, 238. (Link zur Quelle)
- https://www.g-ba.de/downloads/40-268-6231/2019-12-19_MVV-RL_Vakuumversieglungstherapie-Wunden_TrG.pdf (Link zur Quelle)
- Arundel, C., et al. (SWHSI-2 = Surgical Wounds Healing by Secondary Intention-2): Lancet 2025, 405, 1689. (Link zur Quelle)
- Macefield, R., et al.: Br. J. Surg. 2019, 106, 226. (Link zur Quelle)
- Brooks, R., et al.: The measurement and valuation of health status using EQ-5D: a European perspective. Dordrecht: Kluwer Academic Publishers, 2003. (Link zur Quelle)
- https://register.awmf.org/assets/guidelines/091-001e_S3_Lokaltherapie-schwerheilender-chronischer-Wunden_2023-11.pdf (Link zur Quelle)