Die IRMA-II-, IDNT- und RENAAL-Studie
Zusammenfassung: In drei großen Studien haben sich die Angiotensin-II-Rezeptor-Blocker (AT-II-RB) Irbesartan bzw. Losartan als wirksam erwiesen, das Fortschreiten einer Nephropathie bei hypertensiven Typ-2-Diabetikern zu verzögern. Dies betraf sowohl Frühstadien (Mikroalbuminurie) wie auch fortgeschrittene Stadien (große Proteinurie, eingeschränkte Nierenfunktion). Die Wirkung war stärker als es dem Ausmaß der Blutdrucksenkung nach zu erwarten gewesen wäre. Unerwünschte Arzneimittelwirkungen waren selten und nicht gravierend. Ein Nachteil dieser Studien ist, daß ACE-Hemmer nicht mituntersucht wurden, so daß ihre auch bei hypertensiven Typ-2-Diabetikern vermutete renoprotektive Wirksamkeit und ihre Verträglichkeit nicht im direkten Vergleich mit AT-II-RB zu beurteilen ist. Dennoch kann empfohlen werden, die Therapie mit ACE-Hemmern zu beginnen und nur bei UAW (z.B. Husten, angioneurotisches Ödem) auf AT-II-RB umzustellen. Kreatininkontrollen sind zu Beginn der Therapie jedoch engmaschig erforderlich, da es (meist vorübergehend) zu einer Verschlechterung der Nierenfunktion kommen kann, besonders bei bereits fortgeschrittener Niereninsuffizienz.
Bei ca. 40% der Patienten mit Diabetes mellitus Typ 2 entsteht im Laufe von Jahren eine diabetische Nephropathie. Diese Komplikation ist heute mit einem Anteil von 25-40% der Patienten vielerorts die häufigste Ursache für eine dialysepflichtig gewordene Niereninsuffizienz. Das Problem nimmt weltweit zu, weil der Diabetes mellitus häufiger wird (in den USA bereits > 6,5% der Bevölkerung) und weil mehr Patienten wegen der höheren Lebenserwartung Komplikationen des Diabetes mellitus erleben.
Die diabetische Nephropathie beginnt paradoxerweise zunächst mit einer erhöhten glomerulären Filtrationsrate („Hyperfiltration“), die dann im Laufe von Jahren durch Sklerosierungsvorgänge – wahrscheinlich teilweise verursacht durch Angiotensin II – bis zur terminalen Niereninsuffizienz abnimmt. Schlechte Blutzucker-Einstellung und (unzureichend behandelte) arterielle Hypertonie – eine häufige Begleiterkrankung bei Typ-2-Diabetes – erhöhen die Inzidenz dieser Komplikation und beschleunigen ihren Verlauf. Es ist daher im Einzelfall diagnostisch schwer zu entscheiden, in welchen Ausmaß diabetische und/oder hypertensive Schäden an der Niereninsuffizienz beteiligt sind. Als frühes und prognostisch ungünstiges Zeichen einer renalen Beteiligung bei Diabetes mellitus Typ 1 und 2 gilt eine – bereits schon geringe – Albuminurie (sog. Mikroalbuminurie = 20-200 µg/min). Mehrere Studien haben gezeigt, daß bei normotensiven Typ-1-Diabetikern die Blockade des Renin-Angiotensin-Systems mit ACE-Hemmern das Fortschreiten einer Mikroalbuminurie zur Makroalbuminurie – und damit verbunden auch das Fortschreiten der Niereninsuffizienz – verzögern kann und somit diese Substanzklasse unter guter Kontrolle auch zu empfehlen ist (Übersicht bei 1). Entsprechende und ausreichende Daten für hypertensive Typ-2-Diabetiker gibt es bisher nicht. Nun sind im N. Engl. J. Med. an prominenter Stelle gleich drei große Studien erschienen, die sich mit den pathophysiologisch erhofften renoprotektiven Effekten der Angiotensin-II-Rezeptor-Blocker (AT-II-RB) Irbesartan (2, 3) bzw. Losartan (4) bei diesen Patienten befassen. Die Studie wurden bereits im Mai des Jahres auf dem amerikanischen Hypertensiologie-Kongreß vorgestellt (5).
In der IRMA-II-Studie (2; multinational, randomisiert, doppeltblind, plazebokontrolliert; Sponsor: Sanofi-Synthelabo und Bristol-Myers) wurden insgesamt 590 hypertensive Typ-2-Diabetiker mit Mikroalbuminurie (um 55 µg/min) und noch normalem Serum-Kreatinin (Kreatinin-Clearance um 110 ml/min) entweder mit 300 mg/d (n = 194) oder 150 mg/d (n = 195) Irbesartan (Aprovel, Karvea) oder Plazebo (n = 201) zwei Jahre lang behandelt. Die Patienten der drei Gruppen unterschieden sich zu Beginn nicht in wichtigen klinischen Parametern (z.B. Dauer, Art und Güte der Behandlung des Diabetes, Art und Schwere diabetischer Komplikationen, arterielle Hypertonie, Body-Mass-Index u.a.). Die arterielle Hypertonie durfte in allen drei Gruppen zusätzlich zur Studien-Medikation mit Diuretika, Beta-Blockern, Nicht-Dihydropyridin-Kalziumantagonisten und Alpha-Blockern, nicht jedoch mit ACE-Hemmern behandelt werden. Ziel-Blutdruck war 135/85 mmHg nach drei Monaten. Primärer Endpunkt war der Zeitpunkt des Beginns einer diabetischen Nephropathie. Er war definiert als Albuminurie > 200 µg/min.
Ergebnisse: In den Irbesartan-Gruppen erreichten 5,2% (300 mg/d) bzw. 9,7% (150 mg/d) und in der Plazebo-Gruppe 14,9% der Patienten den Endpunkt. Der Unterschied zwischen der Plazebo-Gruppe und der Gruppe mit der höheren Irbesartan-Dosierung war signifikant (p < 0,001). In allen drei Gruppen kam es im Mittel zu einem Rückgang der Mikroalbuminurie: Irbesartan 300 mg/d um 38% (95%-Konfidenzintervall: 32 bis 40%), Irbesartan 150 mg/d um 24% (19 bis 29%), Plazebo 2% (-7 bis +5%). Auffällig war, daß unter der höheren Irbesartan-Dosis die Kreatinin-Clearance zunächst stärker abfiel als in den beiden anderen Gruppen. Nach drei Monaten war dieser Effekt, der möglicherweise intrarenal hämodynamisch zu erklären ist, aber den anderen Gruppen angeglichen. Der Blutdruck war in den Irbesartan-Gruppen am Ende der Studie nur geringfügig niedriger als in der Plazebo-Gruppe (141/83 vs. 143/83 vs. 144/83 mm Hg). Die Autoren schließen aus diesen Ergebnissen, daß Irbesartan - zumindest in der 300 mg-Dosierung - renoprotektiv wirkt und dies wohl teilweise unabhängig von seiner blutdrucksenkenden Wirkung.
In der IDNT-Studie (3; multinational, randomisiert, doppeltblind, plazebokontrolliert; Sponsor: Sanofi-Synthelabo und Bristol-Myers) wurden 1715 ebenfalls hypertensive Patienten mit Typ-2-Diabetes und bereits fortgeschrittener diabetischer Nephropathie (Serum-Kreatinin um 1,7 mg/dl; Proteinurie 2,9 g/24 h, Albuminurie 1,9 g/24 h) im Mittel 2,6 Jahre lang mit 300 mg/d Irbesartan oder 10 mg/d Amlodipin (Norvasc) oder Plazebo behandelt. Der Ziel-Blutdruck war 135/85 mm Hg. Die drei Gruppen unterschieden sich zu Beginn nicht in den wichtigsten klinischen Parametern.
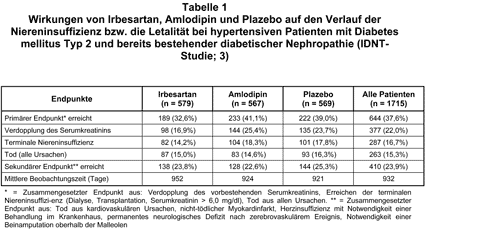
Ergebnisse: Der primäre und der sekundäre Endpunkt sowie die wichtigsten sonstigen Ergebnisse sind in Tab. 1 wiedergegeben. Die Autoren kommen zu dem Schluß, daß Irbesartan das Fortschreiten einer bereits vorhandenen diabetischen Nephropathie mit Niereninsuffizienz verlangsamen kann und daß dieser Schutz unabhängig ist von der blutdrucksenkenden Wirkung des AT-II-RB. Ein Überlebensvorteil ergab sich jedoch nicht. Der Kalziumantagonist Amlodipin unterschied sich nicht von Plazebo. Die Unterschiede in den Gruppen sind im Ergebnisteil der Originalarbeit in absoluten Zahlen und in Kaplan-Meier-Kurven, im Abstract jedoch in Relativ-Prozent (prozentualer Unterschied im Relativen Risiko) angegeben, was bei oberflächlicher Betrachtungsweise leicht dazu führt, die positiven Wirkungen von Irbesartan zu überschätzen (s.a. AMB 1992, 26, 87). So erreichten z.B. den primären Endpunkt unter Irbesartan 32,6% und unter Plazebo 39% der Patienten, d.h. es besteht ein absoluter Unterschied von „nur“ 6,4 Prozentpunkten (s. Tab. 1). Dies sind aber – wenn als Relatives Risiko dargestellt – 0,8 vs. 1,0, also 20% (!) weniger.
In der dritten, der RENAAL-Studie (4; ebenfalls multinational, randomisiert, doppeltblind und plazebokontrolliert; Sponsor: Merck und Co.) wurden 1513 hypertensive Typ-2-Diabetiker mit Niereninsuffizienz (Serum-Kreatinin 1,9 mg/dl) im Mittel 3,4 Jahre lang mit täglich 50-100 mg Losartan (Lorzaar) bzw. Plazebo behandelt.
Ergebnisse: Der primäre Endpunkt war zusammengesetzt aus Verdopplung des Ausgangs-Kreatinins, terminale Niereninsuffizienz oder Tod. Er wurde von 47,1% in der Plazebo- und von 43,5% der Patienten in der Losartan-Gruppe erreicht (Risikoreduktion: 3,6 Prozentpunkte = 16%). Ein Überlebensvorteil ergab sich nicht, jedoch fand sich bei der gemeinsamen Auswertung von Verdopplung des Ausgangs-Kreatinins und terminaler Niereninsuffizienz eine Risikoreduktion von 21%. Die vorbestehende Proteinurie nahm unter Losartan im Vergleich mit Plazebo um 35% ab. Auch diese Autoren kommen zu dem Schluß, daß Losartan unabhängig vom Ausmaß der Blutdrucksenkung renoprotektiv ist. Die Verträglichkeit von Losartan war, ebenso wie die von Irbesartan in IRMA und IDNT, gut.
Ein diese Studien begleitendes Editorial von T.H. Hostetter (6) vom National Institute of Diabetes and Digestive and Kidney Diseases, Bethesda, weist auf die Größe des Problems hin: in den USA haben sich Inzidenz und Prävalenz der Patienten mit terminaler Niereninsuffizienz in den letzten 10 Jahren verdoppelt. Dort werden zur Zeit 300000 Patienten dialysiert und 80000 Patienten leben mit einem Nierentransplantat. Bis zum Jahr 2010 wird sich die Zahl der Patienten, die einer Nierenersatz-Therapie bedürfen, um 175 000 erhöhen, die meisten davon als Folge des Typ-2-Diabetes. Hostetter wertet die Ergebnisse dieser drei Arbeiten als deutlichen Fortschritt und schätzt (wohl optimistisch), daß durch eine frühzeitige Gabe von AT-II-RB etwa zwei Jahre im Fortschreiten der diabetischen Nephropathie bis zur Dialysepflichtigkeit gewonnen werden könnten. Er bedauert jedoch, daß in diese großen und kostspieligen Studien keine ACE-Hemmer, die möglicherweise bei hypertensiven Typ-2-Diabetikern ebenfalls renoprotektiv wirksam sind (7, 8), zum direkten Vergleich einbezogen wurden. Damit fehlen Daten, die im Hinblick auf das Abschätzen von Wirksamkeit, Verträglichkeit und Kosten dringend benötigt werden. Er vermutet, daß die merkantilen Interessen der Pharmaindustrie den direkten Vergleich zwischen ACE-Hemmern und AT-II-RB verhindert haben („trial design blurs into marketing strategy“). Die Patentrechte für ACE-Hemmer laufen nämlich früher aus, und es wird danach mit ihnen weniger zu verdienen sein. Andererseits könnten sich bei einem direkten Vergleich beide Substanzklassen als gleich wirksam erweisen, was dann möglicherweise den Absatz der neueren und teureren AT-II-RB schmälert.
Literatur
- The ACE Inhibitors in Diabetic Nephropathy Trialist Group: Ann. Intern. Med. 2001, 134, 370 ; s.a. AMB 2001, 35, 35.
- Parving, H.-H., et al. (IRMA II = IRbesartan in patients with Type 2 diabetes and MicroAlbuminuria study group): N. Engl. J. Med. 2001, 345, 870.
- Lewis, E.J., et al. (IDNT = Irbesartan Diabetic Nephropathy Trial): N. Engl. J. Med. 2001, 345, 851.
- Brenner, B.M., et al. (RENAAL = Reduction of Endpoints in Non-insulin-dependent diabetes mellitus with the Angiotensin II Antagonist Losartan study): N. Engl. J. Med. 2001, 345, 861.
- AMB 2001, 35, 73.
- Hostetter, T.H.: N. Engl. J. Med. 2001, 345, 910.
- Lacourcière, Y., et al.: Kidney Int. 2000, 58, 762.
- HOPE und MICRO-HOPE (Heart Outcomes Prevention Evaluation study investigators): Lancet 2000, 355, 253 und 2000, 356, 860.