Auf das Prinzip der Zytoprotektion gegen Nebenwirkungen von bestimmten Chemotherapeutika haben wir kürzlich am Beispiel des reduzierten Glutathions zur Prävention der Cisplatin-induzierten Neurotoxizität hingewiesen (s. AMB 1996, 30, 31). Inzwischen sind die Ergebnisse einer randomisierten klinischen Studie mit einer anderen schwefelhaltigen Verbindung, Amifostin (Ethyol), publiziert worden, in der die protektive Wirksamkeit dieser Substanz gegen eine Cyclophosphamid-induzierte Hämatotoxizität bzw. Cisplatin-induzierte Nephro-, Neuro- und Ototoxizität untersucht wurde (Kemp, G., et al.: J. Clin. Oncol. 1996, 14, 2101).
Amifostin, früher bekannt unter der Bezeichnung WR-2721, wurde im Rahmen eines von der US-Armee unterstützten Antistrahlenprogramms entwickelt. Die Substanz zeigte in präklinischen Studien eine protektive Wirkung auf unterschiedliche normale Gewebe gegenüber den zytotoxischen Effekten ionisierender Strahlen und Chemotherapeutika. Amifostin ist ein Prodrug, das in vivo durch membranständige und kapillare alkalische Phosphatase zum aktiven Metaboliten, dem freien Thiol WR-1065, umgewandelt wird. Interessanterweise ist die spezifische Aktivität der membranständigen alkalischen Phosphatase in normalen Zellen deutlich höher als in den Zellmembranen von Tumorzellen, so daß im steady-state nach Gabe von Amifostin eine wesentlich höhere Konzentration an freiem Thiol in normalen Geweben im Vergleich zu Tumorgewebe nachweisbar ist. Nach intrazellulär gelangte Thiol-Gruppen fangen freie Radikale ab, sind an der Reparatur beschädigter intrazellulärer Moleküle beteiligt und wirken als nukleophile Substanzen, die die Alkylierung von Nukleinsäuren hemmen.
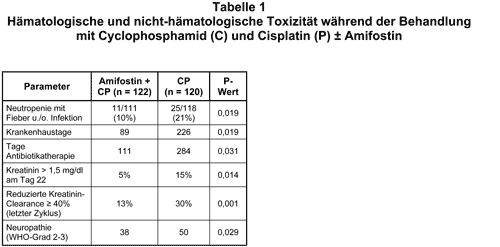
Bisher liegen nur wenige kontrollierte klinische Studien vor, welche die Wirksamkeit dieses interessanten Mechanismus der Zytoprotektiön gegen spezielle Chemotherapeutika gründlich analysiert haben. Die Ergebnisse der obengenannten Phase-lll-Studie, die vom Hersteller des Amifostins, US Bioscience, finanziell unterstützt wurde, sind deshalb von besonderem Interesse. Insgesamt 242 Patientinnen mit fortgeschrittenem Ovarialkarzinom (FIGO Stadium III und IV) wurden aufgenommen und erhielten nach Randomisierung 6 Zyklen einer Chemotherapie mit Cyclophosphamid (1000 mg/m2Körperoberfläche) sowie Cisplatin (100 mg/m2) in dreiwöchigen Abständen mit Amifostin (910 mg/m2als 15minütige i.v. Infusion innerhalb von 30 Minuten vor Cyclophosphamid) bzw. ohne Amifostin. Bei beiden Patientengruppen wurde begleitend eine ausreichende Hydratation mit forcierter Diurese (Mannit) durchgeführt. Die wesentlichen Ergebnisse der Studie sind in Tab. 1 zusammengefaßt und ergeben eine signifikante Reduktion der kumulativen hämatologischen, renalen und neurologischen Toxizität in der mit Amifostin behandelten Patientengruppe. Die Gabe von Amifostin führte auch zu einer, allerdings nicht signifikanten, Abnahme der Cisplatin-induzierten Ototoxizität.
Die Ansprechraten des Ovarialkarzinoms und die mediane Überlebenszeit nach einer medianen Beobachtungsdauer von 41 Monaten unterschieden sich in den beiden Gruppen nicht.
Die wesentlichen, bereits bekannten Nebenwirkungen des Amifostins (Übelkeit, Erbrechen, Hypotension) wurden auch in dieser klinischen Studie beobachtet, wobei 96% der mit Amifostin behandelten Patientinnen und 88% in der Kontroll-Gruppe unter Übelkeit und/oder Erbrechen litten. Bei 75 Patientinnen (61,5%) trat ein systolischer Blutdruckabfall auf, der eine Unterbrechung der Infusion notwendig machte. Durch inzwischen verbesserte antiemetische Therapiestrategien (z.B. mit Dexamethason und Ondansetron) bzw. vorbeugende Maßnahmen gegen die Hypotension (Infusion des Amifostins in sitzender Position) können diese Nebenwirkungen besser beherrscht werden.
Fazit: Bei Patientinnen mit Ovarialkarzinom, die mit Cyclophosphamid und Cisplatin behandelt werden, führt eine gleichzeitige Gabe von Amifostin zur Reduktion der Hämato-, Nephro- und Neurotoxizität ohne Beeinträchtigung der Antitumoraktivität. Aufgrund der beiden häufigsten Nebenwirkungen von Amifostin, Erbrechen und Hypotension, muß auf begleitende Maßnahmen, wie z.B. eine optimale antiemetische Therapie und sorgfältige Überwachung des Blutdrucks, insbesondere bei Patientinnen mit kardiovaskulären bzw. zerebrovaskulären Erkrankungen, geachtet werden. Die Ergebnisse dieser Studie haben in den USA zur Zulassung von Amifostin zur Reduktion des auf Neutropenie beruhenden lnfektionsrisikos bei der Behandlung des fortgeschrittenen Ovarialkarzinoms mit Cisplatin und/oder Cyclophosphamid geführt. Als weiteres Anwendungsgebiet ist Amifostin in Deutschland zum Schutz vor kumulativer Nephrotoxizität bei Patienten mit soliden Tumoren (Keimzelltumoren ausgenommen), die Cisplatin-haltige Therapieregime erhalten, zugelassen.