Venöse Thromboembolien (tiefe Venenthrombose bzw. Lungenembolie) sind seltene Nebenwirkungen kombinierter hormonaler Kontrazeptiva (KOK), die lange bekannt sind ([1], vgl. [2]). Im Jahr 2013 hat die Europäische Arzneimittel-Agentur (EMA) das Verhältnis von Nutzen und Risiko von KOK für die Schwangerschaftsverhütung bewertet ([3], [4]). Dabei wurde für alle in der Europäischen Union als KOK zugelassenen Arzneimittel – neben den sogenannten „Pillen“ auch zur Schwangerschaftsverhütung zugelassene Hormonpflaster und Hormonringe – untersucht, wie hoch das Risiko ist, durch die Anwendung eine venöse Thromboembolie zu erleiden. Außerdem wurde geprüft, ob regulatorische Maßnahmen erfolgen sollten, beispielsweise eine Beschränkung des Anwendungsgebiets dieser Arzneimittel. Die Bewertung ergab unter anderem, dass das Risiko für venöse Thromboembolien bei allen KOK mit niedrigem Ethinylestradiol-Gehalt (< 50 µg) gering ist. Es zeigte sich aber auch, dass sich das Risiko für eine venöse Thromboembolie zwischen den einzelnen KOK in Abhängigkeit vom enthaltenen Gestagen unterscheidet. Präparate mit den Gestagenen Levonorgestrel, Norethisteron oder Norgestimat haben das niedrigste Risiko für venöse Thromboembolien.
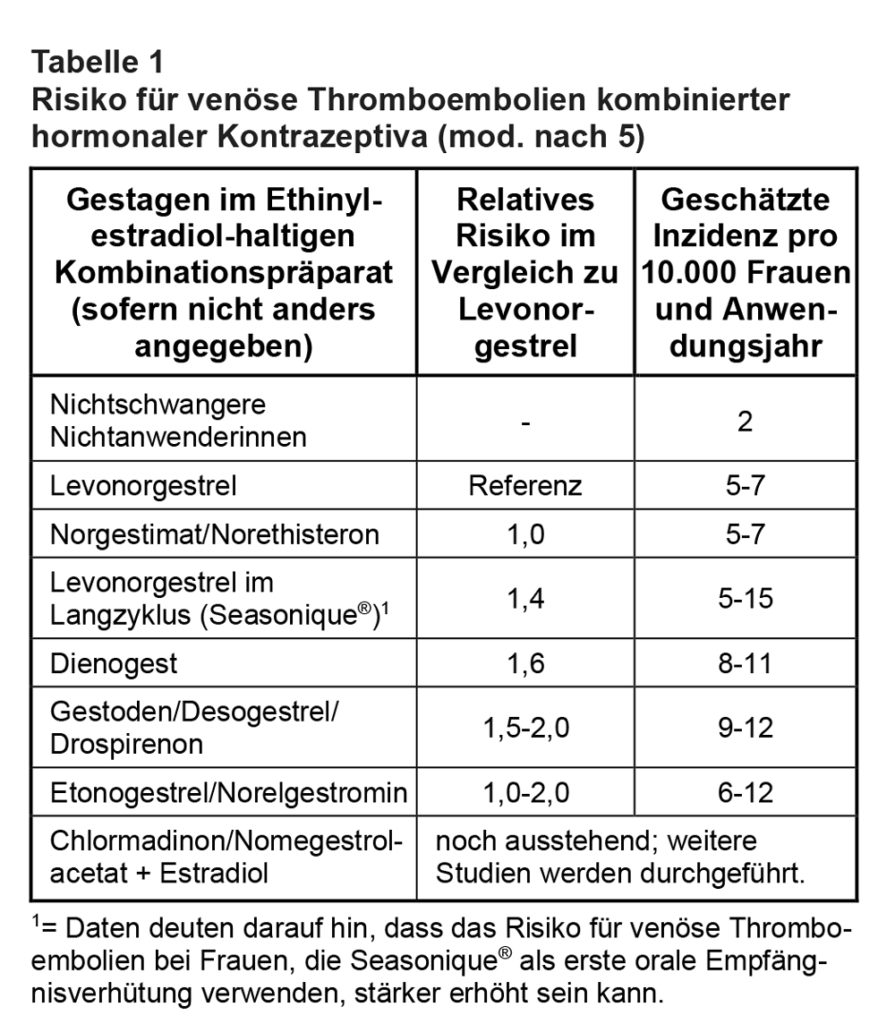
Hinsichtlich des Nutzens fanden sich keine Unterschiede zwischen den einzelnen KOK. Auf der Grundlage neuer Studienergebnisse konnten inzwischen auch die Risiken für die Kombination mit Dienogest sowie Levonorgestrel im Langzyklus (Seasonique®) ermittelt werden, die im Jahr 2013 noch nicht bekannt waren. Darüber informiert das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) nun in einem firmenunabhängigen Rote-Hand-Brief, der auch eine tabellarische Übersicht zum Risiko für venöse Thromboembolien von KOK enthält ([5], s. Tab. 1).
Das Risiko von Thromboembolien unter KOK ist zwar gering, sie können jedoch schwerwiegend und bei 1-2% der Patientinnen auch tödlich verlaufen. So berichtete die Arzneimittelkommission der deutschen Ärzteschaft über eine 22-jährige Frau, die ein Drospirenon-haltiges Kombinationspräparat eingenommen hatte [6]. Risikofaktoren für eine venöse Thromboembolie lagen bei ihr nicht vor. Die Frau brach vor ihrer Haustür plötzlich bewusstlos zusammen. Als Ursache wird von einer fulminanten Lungenembolie ausgegangen, unter anderem aufgrund eines typischen Befunds in einer Echokardiographie, die später im Krankenhaus durchgeführt wurde. Trotz unverzüglich eingeleiteter Reanimationsmaßnahmen durch den Notarzt und eine Notfall-Lysebehandlung im Krankenhaus starb die Patientin. Gemäß einer retrospektiven Befragung von Kontaktpersonen hatte die Frau in den Wochen vor dem Ereignis über Wadenschmerzen geklagt, die sie zunächst auf Radfahren zurückführte und die von ärztlicher Seite als Muskelzerrung interpretiert wurden.
Das BfArM weist darauf hin, dass die Anwenderinnen durch die verschreibenden Ärzte umfänglich über das Risiko von venösen Thromboembolien informiert werden müssen. Das Risiko für eine venöse Thromboembolie ist im ersten Jahr der Anwendung eines KOK und nach erneutem Beginn der Anwendung nach einer Pause von mindestens 4 Wochen am höchsten. Vor der Verschreibung sollten die Frauen darüber aufgeklärt werden, wie sie selbst Anzeichen einer Thrombose erkennen können. Zu den Risikofaktoren für eine venöse Thromboembolie zählen unter anderem Rauchen, Adipositas, Alter > 35 Jahre, Immobilisierung und genetische Prädisposition. Die Risiken für venöse Thromboembolien ändern sich im Laufe des Lebens und müssen daher regelmäßig neu beurteilt werden. Mit den Anwenderinnen sollten persönliche Risikofaktoren besprochen und die Anwendung eines hormonalen Verhütungsmittels individuell abgewogen werden.
Für das Gespräch mit der Patientin stehen auf der Website des BfArM eine Checkliste für die Verschreibung sowie eine Informationskarte für die Patientin zur Verfügung, die allen Patientinnen ausgehändigt werden soll [1]. Das BfArM stellt dar, dass der Beratung durch den Arzt insbesondere dann eine entscheidende Bedeutung zukommt, wenn junge Erstanwenderinnen gezielt nach einem bestimmten hormonalen Verhütungsmittel fragen, ohne sich vorher genauer mit den Risiken befasst zu haben. Die ärztliche Beratung müsse hier darauf abzielen, dass KOK Arzneimittel sind, die mit ernsthaften Risiken verbunden sein können und keine sogenannten Lifestyle-Produkte. Die Verordnung darf nicht aus kosmetischen Gründen erfolgen. Aufgrund der Gewichtsreduktion und verminderten Akneneigung durch die antimineralokortikoide bzw. antiandrogene Wirkung wird bei jungen Frauen häufig die Verordnung Drospirenon-haltiger Präparate erwogen.
Das Risiko für arterielle Embolien, die z.B. zu einem Schlaganfall oder Myokardinfarkt führen können, ist unter KOK ebenfalls erhöht. Angaben zu Unterschieden im Risiko dafür seien aufgrund der Datenlage laut des Rote-Hand-Briefs zurzeit nicht möglich.