Über den optimalen Ziel-Blutdruck (RR) bei Behandlung von Patienten mit arterieller Hypertonie besteht keine Einigkeit [1]. So empfiehlt die Leitlinie der Europäischen Gesellschaft für Kardiologie (ESC) als allgemeines Therapieziel systolische RR-Werte zwischen 130-139 mm Hg ([2], [3]) und das „American College of Cardiology“ sowie die „American Heart Association“ < 130 mm Hg [4]. Unklarheit besteht auch über die optimalen Zielwerte bei älteren Patienten, denn diese Gruppe wurde oft nicht in die Studien eingeschlossen.
In der nordamerikanischen SPRINT-Studie ([5] [6]), über die wir ausführlich berichtet haben (vgl. [7]), wurden zwei unterschiedliche RR-Zielbereiche bei > 9.000 Patienten mit Hypertonie und Alter > 75 Jahre hinsichtlich kardiovaskulärer (kv) Erkrankungen und der Letalität untersucht. In der aggressiver behandelten Gruppe wurde ein systolischer RR-Zielwert von < 120 mm Hg angestrebt, in der Gruppe mit Standardtherapie < 140 mm Hg. Nach 3,26 Jahren zeigte sich im Vergleich zur Standardtherapie eine signifikante Reduktion des kombinierten kv Endpunkts (5,2% vs. 6,8%) und der Gesamtletalität (3,3% vs. 4,5%). Allerdings waren Patienten mit sehr hohem kv Risiko ausgeschlossen, wie beispielsweise solche mit Zustand nach Schlaganfall oder mit Diabetes mellitus. Es wurden in der Gruppe mit dem niedrigeren RR-Zielbereich vermehrt Nebenwirkungen registriert, wie Hypotonie, Synkopen und Elektrolytverschiebungen. Andere Studien kommen hinsichtlich niedrigerer RR-Ziele zu widersprüchlichen Ergebnissen ([8], vgl. [9]). Für Diabetiker [10] sowie für Patienten < 80 Jahre oder solche mit vorausgegangenen kv Ereignissen [11] gibt es sogar Hinweise, dass eine Senkung des systolischen Blutdrucks < 140 mm Hg die Letalität und kv Ereignisse nicht weiter reduziert, sondern tendenziell sogar erhöht. Wir hatten 2015 dafür plädiert, dass künftige Studien und Leitlinien bei den RR-Zielvorgaben mehr als bisher wichtige individuelle Kofaktoren, wie Komorbiditäten, Gebrechlichkeit, Polypharmakotherapie oder die Präferenz des Patienten, berücksichtigen sollten (vgl. [7], [12]).
In der kürzlich publizierten chinesischen STEP-Studie wurde nun erneut der Einfluss einer intensiven RR-Senkung auf kv Ereignisse bei 60-80-Jährigen mit arterieller Hypertonie untersucht [13].
Studiendesign: STEP wurde als prospektive, randomisierte, kontrollierte Studie an 42 Zentren in China durchgeführt. Die Studie wurde aus öffentlichen Mitteln finanziert, die eingesetzten Antihypertensiva von pharmazeutischen Herstellern in China und die RR-Meßgeräte von „Omron Healthcare“ bereitgestellt. Eingeschlossen wurden Personen mit systolischen RR-Werten zwischen 140-190 mm Hg in 3 Screening-Messungen, auch unter antihypertensiver Therapie. Patienten mit ischämischem oder hämorrhagischem Insult in der Anamnese waren ausgeschlossen. Der Einschluss erfolgte im Verlauf des Jahres 2017, und die Nachbeobachtung war über 4 Jahre geplant.
Der systolische RR wurde in der Interventionsgruppe (intensive Therapie = IT) in den Zielbereich von 110 bis < 130 mm Hg gesenkt und in der Vergleichsgruppe (Standardtherapie = ST) in den Zielbereich von 130-150 mm Hg. In die RR-Auswertungen gingen neben den Messungen im Studienzentrum auch die Selbstmessungen in der häuslichen Umgebung ein, um Verzerrungen durch Weißkitteleffekte zu minimieren. Die selbst gemessenen RR-Werte wurden über eine Smartphone-basierte App an das Studienzentrum übermittelt. Darüber hinaus wurden die Teilnehmer nach 1, 2 und 3 Monaten sowie über 4 Jahre alle 3 Monate einbestellt und ihre Vitalwerte, Medikation sowie unerwünschte Wirkungen (UAW) abgefragt. Einmal jährlich erfolgten zudem Blutuntersuchungen. Das kv Risiko wurde mit dem Framingham Risk Score abgeschätzt [14].
Die antihypertensive Therapie erfolgte nach einem festgelegten Behandlungsalgorithmus mit dem hierzulande wenig gebräuchlichen Angiotensin-II-Rezeptor-Blocker Olmesartan, dem Kalziumantagonisten Amlodipin und dem Diuretikum Hydrochlorothiazid.
Primärer Studienendpunkt war die Kombination von ischämischem oder hämorrhagischem Schlaganfall, akutem Koronarsyndrom (Myokardinfarkt oder instabile Angina pectoris mit Krankenhausbehandlung), koronare Revaskularisation, akute kardiale Dekompensation, Vorhofflimmern oder Tod aus kv Ursachen. Sekundäre Endpunkte waren u.a. Tod jeder Ursache sowie die einzelnen kardialen Ereignisse aus dem primären Endpunkt (Schlaganfall ausgenommen) sowie eine Verschlechterung der Nierenfunktion.
Ergebnisse: Von 9.624 gescreenten Patienten wurden 8.511 eingeschlossen. Die IT erhielten 4.243 und die ST 4.268. Die klinischen Kenndaten bei Studienbeginn waren in beiden Armen etwa gleich: 46,5% Männer (zum Vergleich in SPRINT: 72%), mittleres Alter 66,2 Jahre (in SPRINT: 68 Jahre); 76% im Alter von 60-70 Jahren und 24% zwischen 70-80 Jahren. Der Ausgangs-RR betrug in beiden Armen 146/82 mm Hg (in SPRINT: 140/78 mm Hg); auch die Komorbiditäten waren in beiden Armen gleich: 19,1% Diabetiker, 6,3% mit kv Vorerkrankung, mittlerer BMI 25 kg/m2; 64,8% hatten ein hohes kv 10-Jahres Risiko (Framingham Risk Score ≥ 15%).
Die Studie wurde nach einer Interimsanalyse wegen signifikant weniger Endpunkt-Ereignissen im IT-Arm nach einer medianen Laufzeit von 3,34 Jahren am 31.12.2020 vorzeitig beendet. Bei 234 Teilnehmern (2,7%) fehlten Daten für eine vollständige Analyse. Am Ende des ersten Jahres betrug der systolische RR im IT-Arm im Mittel 127,5 mm Hg und im ST-Arm 135,3 mm Hg. Dieser Unterschied zeigte sich sowohl bei den zuhause als auch bei den in den Zentren gemessenen RR-Werten. Im IT- bzw. ST-Arm hatten nach einem Jahr 67% bzw. 70% das vorgegebene RR-Ziel erreicht und nach 3 Jahren 77% bzw. 79%. Im Durchschnitt nahmen die Patienten im IT-Arm zuletzt 1,9 Antihypertensiva ein und im ST-Arm 1,5. Zum Vergleich: In der SPRINT Studie waren dies 2,8 bzw. 1,8.
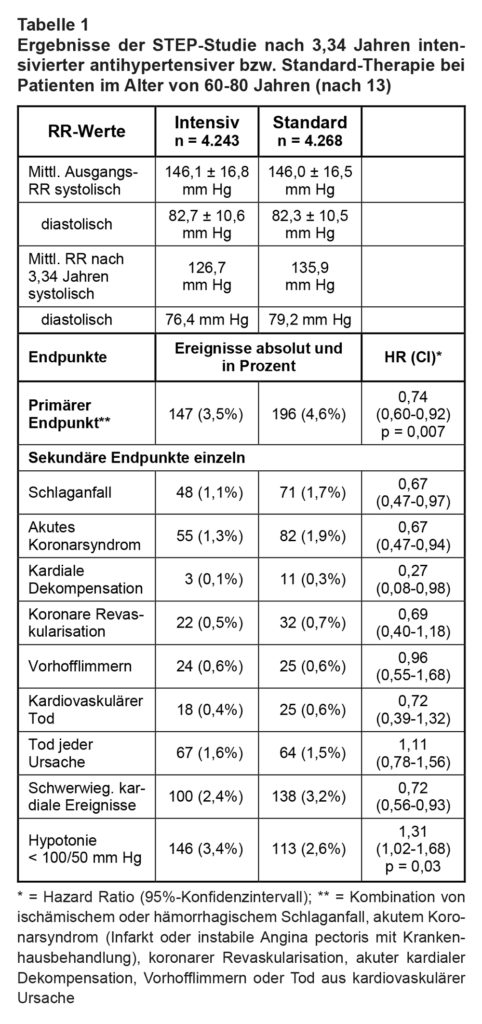
Bei Abbruch der Studie war im IT-Arm bei 147 Patienten (3,5%) und im ST-Arm bei 196 Patienten (4,6%) ein primäres Endpunkt-Ereignis aufgetreten (Hazard Ratio = HR: 0,74; 95%-Konfidenzintervall = CI: 0,60-0,92; p = 0,007). Auch bei den sekundären Endpunkten fanden sich unter IT günstigere Ergebnisse (s. Tab. 1).
Hypotensionen waren im IT-Arm häufiger als im ST-Arm (s. Tab. 1), nicht aber Schwindel, Frakturen, Husten, Angioödeme oder Kopfschmerzen. Die Studienendpunkte Tod aus kv Ursachen oder jedweder Ursache unterschieden sich in beiden Gruppen nicht signifikant.
Diskussion: Wie in SPRINT wirkte sich auch in der STEP-Studie die intensive RR-Senkung bei 60-80-Jährigen günstig auf die Inzidenz kv Ereignisse aus, wie akute Koronarsyndrome, akut dekompensierte Herzinsuffizienz und Schlaganfälle. Es wurden nicht vermehrt UAW registriert, außer Hypotonien: 3,4% vs. 2,6%; in SPRINT waren es 3,4% vs. 2,0%. Der Grund dafür könnte sein, dass für das niedrige RR-Ziel in STEP weniger Antihypertensiva erforderlich waren. Anders als in SPRINT hatte die IT in STEP jedoch keinen signifikant günstigeren Einfluss auf die kv und die Gesamtletalität. Auch andere vergleichbare Studien kamen zu diesem Ergebnis (14
[14] [15] [16] [17]).
Bei der Interpretation und Bewertung der STEP-Ergebnisse gibt es folgende Punkte zu bedenken:
• Die Effekte der intensiveren Behandlung sind insgesamt gering, z.B. Schlaganfall-Inzidenz 0,3% vs. 0,5% pro Jahr. Hieraus errechnet sich die hohe „Number Needed to Treat“ (NNT) von 500 und für dekompensierte Herzinsuffizienz sogar von 1.666.
• Im IT-Arm wurde häufiger mit dem Kalziumantagonisten behandelt als im ST-Arm (63,1% vs. 54,6%), was den günstigeren Verlauf unter IT beeinflusst haben könnte.
• Die kv Ereignisrate war mit 1,0% pro Jahr unter IT und 1,4%/Jahr unter ST niedriger als in der SPRINT-Studie (1,77 bzw. 2,4%/Jahr), was darauf hinweist, dass die Patienten in SPRINT, obwohl Diabetiker ausgeschlossen waren, insgesamt kränker waren, z.B. BMI 30 kg/m2 vs. 25 kg/m2.
• In den Subgruppenanalysen sind die Ergebnisse, bezogen auf den Ausgangsblutdruck, inkonsistent: bei RR ≤ 138 mm Hg betrug die HR für den primären Endpunkt 0,71 (0,48-1,04); bei RR 139-151 mm Hg 0,92 (0,65-1,32) und bei RR ≥ 152 mm Hg 0,62 (0,43-0,89).
• Nur 24% der Studienteilnehmer waren > 70 Jahre alt; drei Viertel waren also vermutlich noch im Berufsleben oder im frühen Rentenalter. Nur 2,4% hatten eine bedeutsame Niereninsuffizienz und nur 6,3% kv Vorerkrankungen. Es handelte sich also um relativ fitte ältere Personen.
• Die Übertragbarkeit der Studienergebnisse auf Europäer ist fraglich. Asiaten haben ein geringeres Risiko für kv Erkrankungen als Europäer und US-Amerikaner ([18], [19]). Der in STEP verwendete Framingham Score (14) basiert auf einer nordamerikanischen Population und überschätzt wahrscheinlich das kv Risiko bei Han-Chinesen ([20] [21] [22]).
• Eine Analyse der Lebensqualität fehlt.
• Olmesartan ist in Europa wenig gebräuchlich; es kann zu Sprue-ähnlichen Durchfällen führen [23].
Der Autor eines begleitenden Editorials fordert, die arterielle Hypertonie zwingend im Kontext mit anderen individuellen kv Risikofaktoren und Komorbiditäten zu sehen und zu behandeln. Wir sollten nicht an der „verkrusteten“ Sichtweise einer isolierten Krankheit festhalten mit einer schematischen generellen Behandlung nach Richtwerten [24].
Fazit
Fazit: Die STEP-Studie zeigt, wie zuvor die SPRINT-Studie, dass eine intensive Senkung hypertensiver Blutdruckwerte mit Ziel-RR < 130 mm Hg auch bei älteren körperlich leistungsfähigen Menschen (hier Han-Chinesen) sicher durchgeführt werden kann. Es wurden weniger Herzinfarkte, dekompensierte Herzinsuffizienz und Schlaganfälle registriert. Die Gesamtletalität wurde allerdings nicht reduziert. Ob noch ältere und gebrechliche hypertensive Patienten mit kognitiven Einschränkungen bzw. nach Schlaganfällen ebenso sicher behandelt werden können und einen Nutzen von der stärkeren Senkung hypertensiver Blutdruckwerte haben, bleibt weiterhin ungewiss. Wir sind davon überzeugt, dass sich RR-Zielwerte nicht am kalendarischen, sondern am biologischen Alter sowie an relevanten Komorbiditäten orientieren sollten, beispielsweise Niereninsuffizienz oder Diabetes mellitus.
Literatur
- NCD-Risk = Non-Communicable Diseases Risk factor collaboration: Lancet 2017, 389, 37. (Link zur Quelle)
- Williams, B., et al.: Eur. Heart J. 2018, 39, 3021. (Link zur Quelle)
- AMB 2018, 52, 76. (Link zur Quelle)
- Whelton, P.K., et al.: J. Am. Coll. Cardiol. 2018, 71, e127. (Link zur Quelle)
- Williamson, J.D., et al. (SPRINT = Systolic Blood PRessure INtervention Trial): JAMA 2016, 315, 2673. (Link zur Quelle)
- Lewis, C.E., et al. (SPRINT = Systolic Blood PRessure INtervention Trial): N. Engl. J. Med. 2021, 384, 1921. (Link zur Quelle)
- AMB 2016, 50, 04. AMB 2015, 49, 89. (Link zur Quelle)
- Ettehad, D., et al.: Lancet 2016, 387, 957. (Link zur Quelle)
- AMB 2018, 52, 68. (Link zur Quelle)
- Brunström, M., und Carlberg, B.: BMJ 2016, 352, i717. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4770818/. Vgl. AMB 2016, 50, 27. (Link zur Quelle)
- Douros, A., et al. (BIS = Berlin Intervention Study): Eur. Heart J. 2019, 40, 2021. (Link zur Quelle)
- AMB 2020, 54, 91. (Link zur Quelle)
- Weili, Z., et al. (STEP = STrategy of blood pressure intervention in the Elderly hypertensive Patients): N. Engl. J. Med. 2021, 385, 1268. (Link zur Quelle)
- D’Agostino, R.B., et al. (FHS = Framingham Heart Study): Circulation 2008, 117, 743. (Link zur Quelle)
- Messerli, F.H., et al.: Circulation 2018, 138, 128. (Link zur Quelle)
- SHEP = Systolic Hypertension in the Elderly Program. JAMA 1991, 265, 3255. https://jamanetwork.com/journals/jama/article-abstract/386293. Vgl. AMB 2007, 41, 27. AMB 1998, 32, 33. (Link zur Quelle)
- Staessen, J.A., et al. (Syst-Eur = Systolic Hypertension in Europe): Lancet 1997, 350, 757. (Link zur Quelle)
-
Beckett, N.S., et al. (HYVET = Hypertension in the Very Elderly Trial): N. Engl. J. Med. 2008, 358, 1887. https://www.nejm.org/doi/10.1056/NEJMoa0801369?url_ver=Z39.88-2003&rfr_id=ori:rid:crossref.org&rfr_dat=cr_pub%20%200www.ncbi.nlm.nih.gov. Vgl. AMB 2015, 49, 20. AMB 2012, 46, 13.
(Link zur Quelle) - Qi, Y., et al.: J. Am. Coll. Cardiol. 2018, 72, 1201. (Link zur Quelle)
- Yusuf, S., et al. (HOPE-3 = Heart Outcomes Prevention Evaluation-3): N. Engl. J. Med. 2016, 374, 2021. (Link zur Quelle)
- Chen, W.W., et al.: J. Geriatr. Cardiol. 2017, 14, 1. (Link zur Quelle)
- Yang, X., et al. (China-PAR Project = Prediction for ASCVD Risk in China): Circulation 2016, 134, 1430. (Link zur Quelle)
- AMB 2013, 47, 63a. (Link zur Quelle)
- Nelson, M.R.: N. Engl. J. Med. 2021, 385, 1328. (Link zur Quelle)