Zusammenfassung
Die Hemmstoffe der PCSK9 zählen zu den wirksamsten und teuersten Lipidsenkern. Sie reduzieren das LDL-Cholesterin um 50-72% und das Lipoprotein (a) um 20-25%. Ihr klinischer Nutzen ist auch 8 Jahre nach der Zulassung der ersten beiden PCSK9-Hemmer nur schwer zu beurteilen. Ein Überlebensvorteil ist nur für Alirocumab nachgewiesen, wenn es zusätzlich zu einem Statin plus/oder Ezetimib gegeben wird. Evolocumab senkt zwar die Rate an Herzinfarkten, Schlaganfällen und Koronar-Revaskularisationen, verlängert jedoch nicht das Überleben. Die Daten für Inclisiran sind weiterhin unzureichend für eine Bewertung. Die Langzeitverträglichkeit der Therapie mit den monoklonalen Antikörpern ist mäßig, aber auf dem Niveau von Plazebo. Etwa ein Viertel der Patienten klagt im ersten Behandlungsjahr über schwerwiegende Nebenwirkungen, und hiernach sind es rund 10% pro Jahr. Mindestens 5% der Studienpatienten brechen die Behandlung mittelfristig wegen Nebenwirkungen ab.
Im Jahr 2015 wurden die humanen monoklonalen Antikörper (mAK) Evolocumab und Alirocumab zur Behandlung der Hypercholesterinämie zugelassen und 5 Jahre später Inclisiran aus der Gruppe der „small interfering RNA“ (siRNA; vgl. [1]). Die beiden mAK können verordnet werden zur Behandlung der primären Hypercholesterinämie und der gemischten Dyslipidämie bei Erwachsenen und Kindern und Jugendlichen im Alter von ≥ 8 bzw.10 Jahren in Kombination mit einem Statin oder einer anderen lipidsenkenden Therapie, wenn die Zielwerte für das LDL-Cholesterin (LDL-C) nicht erreicht werden. Außerdem dürfen sie angewendet werden – allein oder in Kombination mit anderen Lipidsenkern – bei Patienten mit Statin-Intoleranz oder bei manifesten atherosklerotischen kardiovaskulären Erkrankungen [2], [3]. Die Zulassung von Inclisiran ist stärker eingeengt: Kindern und Jugendlichen darf es nicht verordnet werden sowie auch nicht in der Indikation atherosklerotische kardiovaskuläre Erkrankungen [4].
Kosten, Verordnungsvolumen und Rechtsstreit: Inhibitoren der Proproteinkonvertase Subtilisin/Kexin Typ 9 (PCSK9i) sind teure Lipidsenker. Die Jahrestherapiekosten für die drei zugelassenen Wirkstoffe betragen derzeit knapp 5.300 € (Apothekenverkaufspreis nach [5]). Zum Vergleich: 40 mg generisches Atorvastatin kosten rund 80 € pro Jahr. Der hohe Preis und der jeweils nicht nachgewiesene Zusatznutzen (entsprechend der Nutzenbewertung des Gemeinsamen Bundesausschusses; [6]) dürften Gründe dafür sein, dass sich die PCSK9i nicht breit durchgesetzt haben. In Deutschland wurden 2022 insgesamt 10,2 Mio. definierte Tagesdosen („defined daily dose“ = DDD) der beiden mAK verordnet; das entspricht der Behandlung von etwa 28.000 Patienten [7].
Trotz schlechterer Datenlage (s.u.) wurde Evolocumab zuletzt etwa dreimal häufiger verordnet als Alirocumab. Das sind die Folgen eines langjährigen und für pharmazeutische Unternehmer (pU) sehr grundsätzlichen Rechtstreits, in dessen Folge Alirocumab knapp zwei Jahre nicht verfügbar war. Der pU von Evolocumab sah seine Patentrechte verletzt, weil der mAK des Konkurrenten den gleichen molekularen Wirkmechanismus hat. Der Streit wurde im Mai 2023 durch den „U.S. Supreme Court“ mit einem Urteil gegen diese Ansprüche beendet [8].
Wirkweise: Zielstruktur der Hemmstoffe ist die Proproteinkonvertase Subtilisin/Kexin Typ 9 (PCSK9). Dieses Enzym ist maßgeblich am Abbau des LDL-Rezeptors beteiligt. Die mAK binden an zirkulierendes PCSK9 und neutralisieren es; die siRNA verhindert dagegen dessen Synthese im Zellkern. In beiden Fällen resultiert eine Zunahme der LDL-Rezeptoren auf den Leberzellen. Dadurch wird vermehrt LDL-C in die Leber aufgenommen und das zirkulierende LDL-C sinkt. Das Ausmaß der LDL-C-Senkung wird in den Fachinformationen der mAK mit 52-72% und bei Inclisiran mit 50% angegeben. Damit sind sie sehr potente LDL-C-senkende Arzneimittel und liegen im Wirkbereich der Hochdosis-Statin-Therapie bzw. sogar darüber. Außerdem senken die PCSK9i auch das Lipoprotein (a) um 20-25%. Das LDL-C ist aber nur ein Surrogatparameter, und nicht jede LDL-C-Senkung führt zu einem klinischen Nutzen. So reduzieren beispielsweise Östrogen-/Progesteron-Präparate bei postmenopausalen Frauen das LDL-C um 15%. Dies führt jedoch nicht zu einer Abnahme, sondern zu einer leichten Zunahme kardiovaskulärer und thromboembolischer Ereignisse (vgl. [9]). Daher ist bei allen Lipidsenkern stets die wichtige Frage zu stellen, ob sie auch Morbidität und Mortalität senken.
Klinische Effektivität: In der Zeitschrift PLoS One ist kürzlich eine systematische Übersicht und Metaanalyse zu den bis April 2023 publizierten randomisierten, kontrollierten Studien (RCT) mit PCSK9i erschienen [10]. Die Arbeit wurde aus Mitteln des US-amerikanischen „National Institute of General Medicine“ finanziert.
Insgesamt wurden 54 RCT mit 87.669 Studienteilnehmern in die Analyse eingeschlossen. Davon wurden 21 mit Evolocumab, 22 mit Alirocumab und 4 mit Inclisiran durchgeführt. Die Testung erfolgte meist gegen Plazebo und zusätzlich zu einer Basistherapie mit Statinen (70-80%) plus/oder Ezetimib (26-30%). Das mittlere Alter der teilnehmenden Personen lag zwischen 60 und 62 Jahren und der Anteil der Frauen zwischen 33 und 41%.
In den meisten dieser RCT war die Senkung des LDL-C der wichtigste Zielparameter. Nur 24 machen verwertbare Angaben zum Gesamtüberleben und 18 zur kardiovaskulären Mortalität. Die Qualität der RCT mit mAK wird in der Übersicht als gut und das statistische Verzerrungsrisiko als gering bewertet. Die klinischen Daten zu Inclisiran werden dagegen als unzureichend eingestuft, und es ergaben sich auch Hinweise auf einen Publikationsbias.
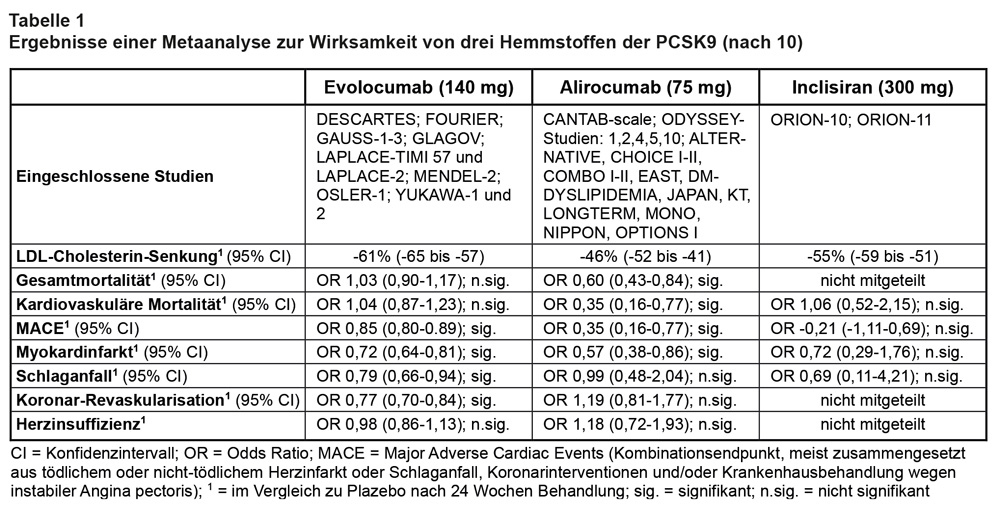
Die Ergebnisse der Metaanalyse sind in Tab. 1 wiedergegeben. Demnach ist das Ausmaß der LDL-C-Senkung mit Evolocumab am größten und mit Alirocumab am geringsten. Nur Alirocumab senkt die Gesamt- und die kardiovaskuläre Mortalität. Für Inclisiran existiert kein Nutzennachweis. Evolocumab senkt die Rate an Herzinfarkten, Schlaganfällen und Koronar-Revaskularisationen; dies hat jedoch keine günstigen Auswirkungen auf die kardiovaskuläre Mortalität. Diese schwer erklärliche Diskrepanz war bereits Inhalt heftiger Diskussionen (vgl. [11]).
PCSK9i wurden aus ethischen Gründen nie gegen Statine getestet. Ob sie vergleichbare Effekte auf Morbidität und Mortalität haben, ist daher ungewiss. Die wenigen RCT mit Statin-intoleranten Patienten (ODYSSEY ALTERNATIVE und GAUSS-3) sind klein, und die gewählten Endpunkte waren LDL-C-Senkung und Verträglichkeit.
Daten zur Langzeitbehandlung und zur Sicherheit: Alle PCSK9i werden von ihren pU in Langzeitstudien weiter untersucht: Evolocumab u.a. in der FOURIER-OLE- [12], Alirocumab u.a. in der ODYSSEY LONG TERM- [13] und Inclisiran u.a. in der ORION-8-Studie (nicht publiziert).
Am aussagekräftigsten ist die Studie ODYSSEY LONG TERM. In dieser Verlängerung der knapp 3-jährigen ODYSSEY OUTCOMES-Studie [14] wird Alirocumab bei 8.242 Patienten weiter verblindet gegen Plazebo getestet. Demnach bleibt die Gesamtsterblichkeit mit Alirocumab auch nach 4 Jahren absolut um 1,6% geringer als mit Plazebo (5,4% vs. 7,0%; p = 0,01). Es errechnet sich eine „Number Needed to Treat“ (NNT) von 62, um einen Todesfall zu verhindern. Auch die sog „MACE-Rate“ (eine Kombination aus tödlichem und nicht-tödlichem Myokardinfarkt oder Schlaganfall und Hospitalisierung wegen instabiler Angina pectoris) ist absolut um 2,2% geringer (NNT 45).
Nach der Sicherheitsanalyse erleiden gleich viele Patienten mit Alirocumab wie mit Plazebo über 4 Jahre mindestens ein unerwünschtes Ereignis (UAE): 78,3% vs. 80,2%. Gut ein Viertel (27,5% bzw. 29,4%) dieser UAE wurde als schwerwiegend beurteilt, und auch ein Absetzen wegen UAE kam gleich häufig vor (4,5%). Die wichtigsten UAE waren ein neu aufgetretener (ca. 11%) oder sich verschlechternder Diabetes mellitus (ca. 20%), neurokognitive Ereignisse (ca. 2%) und Anstieg der Transaminasen (ca. 2%) oder der CK (0,5%), wobei eine systematische Untersuchung auf Demenz oder Katarakt offenbar nicht stattfindet. Alirocumab war gegenüber Plazebo nur bei den lokalen Reaktionen an der Injektionsstelle (5%) im Nachteil.
Daten zur Langzeitsicherheit von Evolocumab kommen aus der offenen FOURIER-OLE-Studie, die bei 6.635 Patienten (24%) ohne Plazebo-Kontrolle als Kohortenstudie weitergeführt wird [12]. Die Autoren versuchen durch vergleichende Analysen von Subkohorten auch Belege für positive Effekte auf das Überleben abzuleiten – beispielsweise bei längerer Therapiedauer oder bei sehr niedrigen erzielten LDL-C-Werten –, was u.E. jedoch nur eine geringe Beweiskraft hat.
In FOURIER [15] hatten in den ersten 48 Wochen 77% ein UAE, 24% ein schwerwiegendes UAE und 1,6% brachen die Behandlung deshalb ab (kein Unterschied zwischen Verum und Plazebo). Die häufigsten UAE waren ein neu diagnostizierter Diabetes mellitus (8,1%), Muskelbeschwerden (5%), allergische Reaktionen (3,1%) und Entzündungen im Bereich der Injektionsstelle (2,1%). In der Verlängerungsstudie beträgt die mediane Nachbeobachtungszeit mittlerweile 5 Jahre, die längste Evolocumab-Therapie 8,4 Jahre. Die Rate schwerwiegender UAE beträgt in dieser selektierten Kohorte durchschnittlich 10,2% pro Jahr. Dabei handelt es sich um Muskelbeschwerden und einen neu diagnostizierten Diabetes mellitus (je 1,2%), Katarakte (0,74%), neurokognitive Ereignisse und allergische Reaktionen (je 0,5%). Die Behandlung beendeten 14,8%, davon 4,2% wegen UAE. Die Langzeitadhärenz mit Evolocumab wurde u.a. in der europäischen HEYMANS-Registerstudie untersucht. Diese liegt nach 30 Monaten bei 92% [16].
Literatur
- AMB 2015, 49, 74. AMB 2021, 55, 97. (Link zur Quelle)
- Fachinformationen Repatha: https://fachkreise.amgen.de/Produkte/Repatha/index.html (Zugriff am 3.1.2024). (Link zur Quelle)
- Fachinformationen Praluent: https://mein.sanofi.de/produkte/praluent (Zugriff am 3.1.2024). (Link zur Quelle)
- Fachinformationen Leqvio: https://klinischeforschung.novartis.de/dokumente/fachinformationen-leqvio-284-mg-injektionsloesung-in-einer-fertigspritze/ (Zugriff am 3.1.2024). (Link zur Quelle)
- https://www.gelbe-liste.de/ (Zugriff am 3.1.2024). (Link zur Quelle)
- Gemeinsamer Bundesausschuss, Nutzenbewertung nach § 35a SGB V für Evolocumab (9.3.2016), Alirocumab (4.5.2016) und Inclisiran (15.7.2021). (Link zur Quelle)
- Schirmer, B., und Schuler, J.: Lipidstoffwechselstörungen. In Ludwig, W.-D., Mühlbauer, B., Seifert, R. (Hrsg.): Arzneiverordnungs-Report 2023. Springer Verlag Berlin (im Druck). (Link zur Quelle)
- https://www.reuters.com/legal/us-supreme-court-rules-against-amgen-bid-revive-cholesterol-drug-patents-2023-05-18/ (Link zur Quelle)
- AMB 2002, 36, 68. AMB 2016, 50, 55. (Link zur Quelle)
- Imran, T.F., et al.: PLoS One 2023, 18, e0295359. (Link zur Quelle)
- AMB 2023, 57, 16DB01. (Link zur Quelle)
- O'Donoghue, M.L., et al. (FOURIER = Further cardiovascular OUtcomes Research with PCSK9 Inhibition in subjects with Elevated Risk): Circulation 2022, 146, 1109. (Link zur Quelle)
- Goodman, S.G., et al. (ODYSSEY OUTCOMES = Evaluation of cardiovascular outcomes after an acute coronary syndrome during treatment with alirocumab): J. Am. Heart Assoc. 2023, 12, e029216. (Link zur Quelle)
- Schwartz, G.G., et al. (ODYSSEY OUTCOMES = Evaluation of cardiovascular outcomes after an acute coronary syndrome during treatment with alirocumab): N. Engl. J. Med. 2018, 379, 2097. (Link zur Quelle)
- Sabatine, M.S., et al. (FOURIER = Further cardiovascular OUtcomes Research with PCSK9 Inhibition in subjects with Elevated Risk): N. Engl. J. Med. 2017, 376, 1713. (Link zur Quelle)
- Ray, K.K. (HEYMANS = Chart Review of Repatha® in Subjects With Hyperlipidaemia): Atherosclerosis 2023, 366, 14. (Link zur Quelle)