Zusammenfassung: Fehler bei der Arzneimitteltherapie gehören zu den wichtigsten Qualitätsmängeln bei stationärer Krankenversorgung. Sie treten besonders an Schnittstellen der Versorgung auf, wo naturgemäß viele Informationen übergeben und bewertet werden müssen, z.B. Schichtwechsel des Personals oder Verlegungen und Entlassungen von Patienten. Außerdem sind sie abhängig von der Qualifikation der Handelnden, den lokalen Arbeitsabläufen und der Komplexität der jeweiligen Behandlungssituation. Deshalb sollte sich jedes Krankenhaus in eigenen Qualitätsanalysen ein Bild über Mängel verschaffen. Ohne strukturierte Analysen lassen sich solche Fehler nicht entdecken und ohne gezielte Maßnahmen kaum verhindern. Solche Maßnahmen sind inzwischen ein Qualitätsmerkmal einer Institution. Kontrollen und Analysen der kritischen Prozesse, z.B. Verordnung und Verabreichung von Arzneimitteln, haben sich bewährt. Sie vermitteln innerhalb kurzer Zeit und mit wenig Aufwand umfassenden Einblick in relevante Abläufe. Elektronische Hilfestellung als Teil der Strategie zur Fehlervermeidung ist inzwischen üblich.
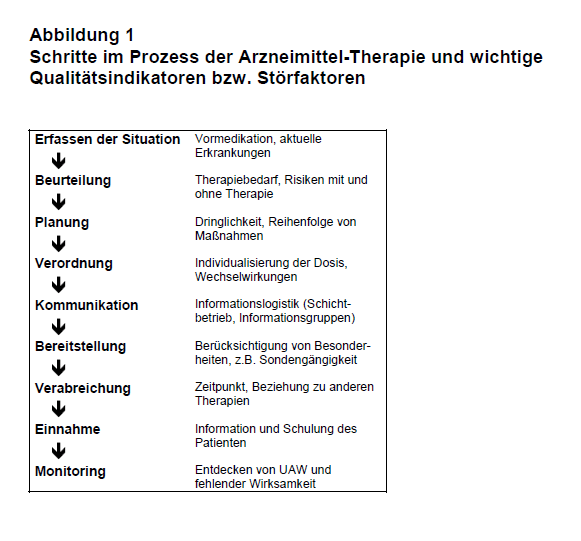
Einleitung: Arzneimitteltherapiesicherheit (AMTS) resultiert aus einer Kette von Analysen, Planungen, Gewichtungen, Entscheidungen und konsequenten Handlungen mit dem Ziel, den Nutzen einer Arzneimitteltherapie für den individuellen Patienten zu maximieren (Abb. 1). Dies bedeutet, dass auch unter schwierigen Bedingungen, wie Zeitdruck, Hektik, Beteiligung vieler Personen, Komplexität der Anforderungen (Multimorbidität, Polypharmakotherapie) und angesichts der Maßnahmen (schwierige oder aufwändige Arzneimittel-Applikation), ausreichend Informationen und Kenntnisse vorliegen müssen. Erst dann können Gefahren durch unterlassenen oder fehlerhaften Arzneimitteleinsatz vermieden werden. Sind diese Informationen und Kenntnisse nicht verfügbar, wird entsprechende Unterstützung notwendig. Wird diese nicht gewährt, kann das Resultat nicht optimal sein.
Maßnahmen zur AMTS sind besonders wichtig bei multimorbiden Patienten mit Polypharmakotherapie (z.B. Intensivpatienten) und an Schnittstellen von Versorgungssektoren, da hier eine umfassende Beurteilung mit Sichtung meist großer Datenmengen erforderlich ist (Schichtwechsel, Aufnahme- und Entlassungsmanagement).
Immer wenn therapierelevante Details unberücksichtigt bleiben, geschehen Fehler. Zwar wird nur eine Minderheit dieser Fehler schwerwiegende Folgen (z.B. vermeidbare unerwünschte Wirkung oder fehlende Wirkung) haben. Da es aber im Einzelfall schwierig ist, die Relevanz solcher Fehler einzuschätzen, sind systematische Strategien notwendig, um grundsätzlich Fehler zu vermeiden.
Entdeckung von Lücken in der AMTS: Jede Institution braucht eigene Daten: Lücken in der AMTS einer Institution sind nicht zwingend auf andere Krankenhäuser übertragbar, denn der lokale Unterstützungsbedarf im Prozess der Arzneimitteltherapie hängt von der Qualifikation der Handelnden, der Verfügbarkeit von Information und der Struktur des Therapieprozesses am Standort ab. Daraus folgt, dass außer bei offensichtlichen Schwächen (z.B. fehlendem problemlosen Zugang zu aktueller – am besten elektronischer – Arzneimittelinformation) eine Institution erst mit einer gezielten Analyse der tatsächlichen Abläufe Klarheit über Art und Ausmaß der Probleme erhält.
Fehler müssen gewichtet werden: Da nicht jeder Fehler mit dem gleichen Risiko verbunden ist, sind Strategien nötig, um die erkannten Schwächen nach Schweregrad und Lösungsmöglichkeiten zu gewichten (1). Mit solchen Analysen kann festgelegt werden, wo Interventionsbedarf besteht und welche Intervention die größte Aussicht auf Erfolg hat. Um Fehler zu erkennen, hat sich in vielen Fällen die direkte Kontrolle durch qualifizierte Personen bewährt. So können tausende verschiedener Verabreichungsprozesse sehr rasch, d.h. innerhalb weniger Wochen, evaluiert werden (1-3). Außerdem können durch Aktivierung der Eigenberichterstattung oder der Spontanmeldesysteme, aber auch durch klinische Pharmazeuten auf den Stationen Risiken entdeckt werden (4, 5). Strukturierte Interviews zur Analyse von Sicherheitsmängeln (z.B. bei jedem Auftreten von UAW) können wertvolle Hinweise auf Systemfehler geben (6). Je nach Ziel ist schließlich auch die Analyse papierbasierter Dokumentation (4, 7-9) oder elektronisch verfügbarer Verordnungsdaten hilfreich (10, 11). Letztere bietet die Möglichkeit, kontinuierlich und automatisiert bei Fehlern zu intervenieren und den Erfolg einer Intervention auch kontinuierlich zu messen (11, 12). Außerdem können Überprüfungen (z.B. in Form von Fragebögen) darüber informieren, ob relevante Inhalte unbekannt sind oder aus anderen Gründen nicht berücksichtigt werden. Wenn Fehlerquellen im Team wohl bekannt sind (z.B. bei steriler Infusionszubereitung), aber trotzdem nicht abgestellt werden, ist es besser, den Arbeitsablauf zu verändern (z.B. weniger Hektik, Möglichkeit der Händedesinfektion am Arbeitsplatz schaffen usw.), als Energie in Fort- und Weiterbildung zu stecken.
Interventionen zur Erhöhung der AMTS: Verschiedene Interventionstechniken haben sich in der Qualitätssicherung der Arzneimitteltherapie als wirksam erwiesen. Den klinischen Systemen zur Entscheidungsunterstützung („Clinical Decision Support Systems” = CDSS) kommt dabei besondere Bedeutung zu. Manuell oder elektronisch unterstützt bieten sie Entscheidungshilfen und Erinnerungsfunktionen unter Berücksichtigung patientenspezifischer Merkmale (13, 40). Häufig sind sie verknüpft mit CPOE-Systemen („Computerized Physician Order Entry”- oder „Computerized Provider Order Entry”-Systeme). Dies sind rechnergestützte Verordnungssysteme, mit dem Ziel, die Zahl von Medikationsfehlern zu vermindern (40). Für den Erfolg der CDSS wurden vier zentrale Voraussetzungen identifiziert. Sind sie gemeinsam vorhanden, ist in 94% ein Erfolg garantiert. Entscheidend sind 1. die Integration in den klinischen Arbeitsprozess mit 2. Unterstützung am Ort und zum Zeitpunkt der Entscheidungsfindung, 3. die automatische Ausgabe einer klaren Handlungsempfehlung (statt alleinige Benachrichtigung über Mängel ohne Lösungsvorschlag) und 4. die Nutzung der Computertechnologie (14, 38). Die Art eines Fehlers beeinflusst auch den Erfolg einer Technik zur Fehlervermeidung. Naturgemäß ist es schwieriger, dezentrale Prozesse, wie die Applikation von Arzneimitteln, elektronisch zu beeinflussen, während die Verordnung von Arzneimitteln elektronischen Interventionen leichter zugänglich ist (11-13, 15, 39).
Risikosituationen im Krankenhaus: AMTS zu erreichen, ist nicht in jeder Behandlungssituation gleich aufwändig. Es gibt Patienten mit besonderem Betreuungsbedarf: Multimorbidität und daraus resultierende Polypharmakotherapie komplizieren die Arzneimitteltherapie für den verschreibenden Arzt und den Patienten. Interaktionen müssen berücksichtigt und individuelle Dosierungen berechnet werden. Adhärenz-fördernde Maßnahmen können notwendig werden. In der stationären Krankenversorgung ergeben sich besonders auf Intensivstationen Probleme mit UAW durch unberücksichtigte Wechselwirkungen (16) und auf pädiatrischen Stationen durch besondere Herausforderungen bei der Applikation (2, 39).
Besondere Risiken bei Schnittstellen: In der AMTS kommt neben den Krankenstationen mit großem Arzneimittelbedarf den Schnittstellen im Versorgungsprozess besondere Bedeutung zu. Therapien werden kompliziert, wenn Patienten von mehreren Ärzten betreut werden müssen: Unterschiedliche Rahmenbedingungen bei der Versorgung (hausärztliche Versorgung versus stationäre Medizin), andere Entgeltsysteme (z.B. DRG), unterschiedliche Arzneimittelsortimente, differierende Aufträge (Langzeitbetreuung vs. Akutmedizin) führen zu unterschiedlichen Interessen. Bei Übertritt Hausarzt/Krankenhaus sind Entscheidungen zu treffen, die beiden gerecht werden und die Bedürfnisse der Patienten in den Vordergrund stellen müssen, ohne die Rahmenbedingungen ihrer Betreuer zu ignorieren (17). Außerdem ist in der stationären Medizin typisch, dass mehrere Personen und Berufsgruppen Einfluss auf die Therapie haben. Deshalb muss der Informationsfluss optimal sein. In der Pharmakotherapie geht es darum, eine etablierte und in der Dosierung bereits titrierte Behandlung nicht zu gefährden und die Durchführbarkeit den Bedürfnissen des Patienten anzupassen.
Jede Schnittstelle zwischen betreuenden Personen kann die Kontinuität einer Therapie gefährden. Deshalb sind Maßnahmen zur Therapieoptimierung besonders wichtig. Solche Maßnahmen umfassen u.a.
· Techniken zur intensiveren Erhebung der Arzneimittel-Anamnese, denn sie ist oft lückenhaft (18-20),
· Standards zum Umsetzen von Therapien auf das jeweilige Arzneimittelsortiment, so genanntes Switching, z.B. auf eine Krankenhausliste (21, 22),
· die Berücksichtigung häufig wechselnder, dosierungsrelevanter Patientenfaktoren, z.B. Nierenfunktion (23-26) und Interaktionen (16), um Über- oder Fehldosierungen zu vermeiden (10, 12),
· Prüfung der technischen (27, 28) und mentalen Durchführbarkeit einer (Kombinations-)Therapie durch den Patienten oder seine Betreuer (2) und eventuell der Vereinfachung des Therapieplans zur Unterstützung der Adhärenz (29),
· strukturiertes Entlassungsmanagement (20, 30), d.h. rasche Information des Hausarztes und Monitoring eventueller UAW (31).
Darüber hinaus ergibt sich bei jedem Wechsel des betreuenden Teams auch eine Chance zur Verbesserung der Qualität, z.B. durch Korrektur von Leitlinienabweichungen (26, 32) oder Dosierungs- und anderen Verordnungsfehlern (11, 12).
Ergebnisse vor und nach Maßnahmen, die AMTS zu verbessern: Aus vielen nationalen und internationalen Studien ist bekannt, dass klinische Systeme zur Entscheidungsunterstützung (CDSS, CPOE s.o.) die Verordnungsqualität erhöhen können (14, 33). Endpunktdaten sind aber noch spärlich (34, 40) und gelegentlich können solche elektronischen Systeme auch gravierende neue Fehler verursachen (35, 36). Es ist deshalb wichtig, dass ein System sorgfältig im klinischen Alltag geprüft wurde.
Situation in Deutschland: Auch in Deutschland haben zahlreiche Studien gezeigt, dass ohne gezielte Maßnahmen sehr viele Fehler im Prozess der Arzneimitteltherapie auftreten und die aktuellen Maßnahmen zur Qualitätssicherung nicht ausreichen. Besonders viele Daten zur Qualität der Arzneimitteltherapie und zur Wirksamkeit entsprechender Interventionen gibt es aus Heidelberg. So wurden Dosierungen oft nicht individualisiert, z.B. bei 48% der Intensivpatienten nicht an die Nierenfunktion angepasst. Nach Intervention waren es 24% (24); 4,8% der Verordnungen waren überdosiert, nach Intervention 3,8% (12); 2,7% der oralen Arzneimittel wurden als teilbare Tabletten verschrieben, obwohl sie nicht teilbar waren. Nach Intervention waren es 1,4% (11). Auf Intensivstation blieben gefährliche Wechselwirkungen in 44% unberücksichtigt (16). Gezielte qualitätssichernde Maßnahmen mit elektronischer und/oder klinisch-pharmazeutischer Unterstützung führten in der Regel mindestens zu einer Halbierung der Fehler und – bei Beachten und Verhindern von Wechselwirkungen – auch der UAW (auf 25%; 16).
Außerdem wurde eine Fülle von Daten zur Verabreichung von Arzneimitteln erhoben. Sie weist darauf hin, dass gut verordnet nicht gleichbedeutend ist mit richtig verabreicht. So waren 5,8% der Infusionen auf Intensivstationen inkompatibel. Nach Intervention: 2,4% nach acht Wochen, 1,2% nach einem Jahr (3, 37). Analysen auf internistischen Stationen entdeckten bei der Zubereitung pro Infusion im Mittel 1,3 und bei der Verabreichung 0,7 Fehler. Beträchtliche Fehlerraten gab es auch bei oralen Arzneimitteln: 0,5 Fehler bei der Zubereitung, 0,2 Fehler bei der Verabreichung (1). Wurden Angehörige (z.B. Eltern) ins Monitoring miteinbezogen, waren nahezu alle (97%) Verabreichungen fehlerhaft (nach Intervention: 5,6%; 2). Das unterstreicht wiederum die Dringlichkeit von Interventionen in diesem Bereich, um die Qualität zu steigern und alle Beteiligten kontrolliert mit einzubeziehen.
Im Krankenhaus treten die Fehler beim Umgang mit Arzneimitteln nicht ausschließlich bei der Verordnung, sondern viel häufiger bei der Applikation auf. Je nach den Rahmenbedingungen in der jeweiligen Institution können diese Fehler durch direkte Intervention oder auch durch elektronische CDSS beträchtlich und relevant vermindert werden, d.h. Halbierung (3, 11, 15, 16, 23) oder mehr (2, 32). Es gibt also erhebliches Verbesserungspotenzial. Wer in seinem Verantwortungsbereich solche Fehler nicht aktiv sucht, muss davon ausgehen, dass viele Fehler unentdeckt bleiben und somit die Qualität nicht verbessert werden kann.
Literatur
- Bertsche, T., et al.: Pharm. World. Sci. 2008, 30, 907. Link zur Quelle
- Bertsche, T., et al.: Qual. Saf. Health Care 2010 (im Druck). Link zur Quelle
- Bertsche, T., et al.: Am. J. Health Syst. Pharm. 2008, 65, 1834. Link zur Quelle
- Bates, D.W., et al.: JAMA 1995, 274, 29. Link zur Quelle
- Schlienger, R.G., et al.: Pharm. World Sci. 1999, 21, 110. Link zur Quelle
- Leape, L.L., et al.: JAMA 1995, 274, 35. Link zur Quelle
- Lesar, T.S., et al.: JAMA 1997, 277, 312. Link zur Quelle
- Knaup, P., et al.: Methods Inf. Med. 2006, 45, 336. Link zur Quelle
- Benkhaial, A., et al.: Pharm. World Sci. 2009, 31, 464. Link zur Quelle
- Seidling, H.M., et al.: Eur. J. Clin. Pharmacol. 2007, 63, 1185. Link zur Quelle
- Quinzler, R., et al.: BMC Med. Inform. Decis. Mak. 2009, 9, 30. Link zur Quelle
- Seidling, H.M., et al.: Qual. Saf. Health Care 2010 (im Druck). Link zur Quelle
- Agrawal, A.: Br. J. Clin. Pharmacol. 2009, 67, 681. Link zur Quelle
- Kawamoto, K., et al.: BMJ 2005, 330, 765. Link zur Quelle
- Bates, D.W., et al.: JAMA1998, 280, 1311. Link zur Quelle
- Bertsche, T., et al.: Intensive Care Med. 2010, 36, 665. Link zur Quelle
- Bertsche, T., et al.: Krankenhauspharmazie 2008, 29, 163.
- Martin-Facklam, M., et al.: Br. J. Clin. Pharmacol. 2004, 58, 437. Link zur Quelle
- Rieger, K., et al.: Eur. J. Clin. Pharmacol. 2004, 60, 363. Link zur Quelle
- Vira, T., et al.: Qual. Saf. Health Care 2006, 15, 122. Link zur Quelle
- Walk, S.U., et al.: Eur. J. Clin. Pharmacol. 2008, 64, 319. Link zur Quelle
- Himmel, W., et al.: Int. J. Clin. Pharmacol. Ther. 2004, 42, 103. Link zur Quelle
- Falconnier, A.D., et al.: J. Gen. Intern. Med. 2001, 16, 369. Link zur Quelle
- Bertsche, T., et al.: Eur. J. Clin. Pharmacol. 2009, 65, 823. Link zur Quelle
- Wong, N.A., und Jones, H.W.: Postgrad. Med. J. 1998, 74, 420. Link zur Quelle
- Pillans, P.I., et al.: Intern. Med. J. 2003, 33, 10 Link zur Quelle. Erratum: Intern. Med. J. 2003, 33, 331.
- Atkin, P.A., et al.: Age Aging 1994, 23, 113. Link zur Quelle
- Quinzler, R., et al.: Eur. J. Clin. Pharmacol. 2006, 62, 1065. Link zur Quelle
- Muir, A.J., et al.: J. Gen. Intern. Med. 2001, 16, 77. Link zur Quelle
- Walker, P.C., et al.: Arch. Intern. Med. 2009, 169, 2003. Link zur Quelle
- Forster, A.J., et al.: Ann. Intern. Med. 2003, 138, 161. Link zur Quelle
- Bertsche, T., et al.: Pain 2009, 147, 20. Link zur Quelle
- Kaushal, R., et al.: Arch. Intern. Med. 2003, 163, 1409. Link zur Quelle
- Garg, A.X., et al.: JAMA 2005, 293, 1223. Link zur Quelle
- Koppel, R., et al.: JAMA 2005, 293, 1197. Link zur Quelle
- Han, Y.Y., et al.: Pediatrics 2005, 116, 1506 Link zur Quelle. Erratum: Pediatrics 2006, 117, 594.
- Bertsche, T., et. al.: Am. J. Health Syst. Pharm. 2009, 66, 1250. Link zur Quelle
- Pearson, S.-A., et al.: BMC Health Serv. Res. 2009, 9, 154. Link zur Quelle
- AMB 2008, 42, 41. Link zur Quelle
- Wille, H., et al.: Link zur Quelle (Zuletzt geprüft am 10.6.2010).