COVID-19 kann gelegentlich mit Myokarditis verlaufen (1). So konnten bei 1% durchtrainierter Athleten mit mildem COVID-19 im Kardio-MRT Hinweise für eine Myokarditis gefunden werden (2, 3). Unklar ist, wie häufig eine Myokarditis auch nach einer Impfung mit mRNA-Impfstoffen gegen SARS-CoV-2 auftreten kann. Bisher gab es hierzu nur publizierte Einzelfallberichte. In das „Vaccine Adverse Event Reporting System“ (VAERS) der US-amerikanischen „Centers for Disease Control and Prevention“ (CDC) sind bis 11. Juni 2021 aber bereits 1.226 Meldungen über Myokarditis nach Impfung mRNA-Vakzinen eingegangen (4, vgl. 19). Das mediane Alter der betroffenen Personen ist 26 Jahre (Spanne: 12-94 Jahre), mehr als zwei Drittel sind Männer (n = 923), und bei ebenfalls zwei Dritteln trat das Ereignis nach der 2. Impfung auf. Eine Subgruppe von 323 jungen Personen (medianes Alter 19 Jahre), bei denen die Diagnose Myokarditis als wahrscheinlich angesehen wurde, wurde von den CDC genauer untersucht. Da 96% im Krankenhaus behandelt wurden, sind die Kriterien einer schwerwiegenden Nebenwirkung erfüllt. Der klinische Verlauf wird als mild beschrieben, und 95% waren zum Zeitpunkt der Analyse wieder entlassen; es gab keinen Todesfall. Bis zu diesem Zeitpunkt waren in den USA etwa 296 Mio. Dosen mRNA-COVID-19-Impfstoffe verabreicht worden, davon 52 Mio. an Personen im Alter von 12-29 Jahren (30 Mio. Erst- und 22 Mio. Zweitimpfungen). Eine mRNA-Vakzin-assoziierte Myokarditis ist also wahrscheinlich sehr selten; verlässliche Aussagen zur Inzidenz sind derzeit noch nicht möglich.
Impfstoff-induzierte Myokarditiden wurden u.a. nach Pockenimpfung (5) und nach Influenzaimpfung beschrieben (6). Bislang wurde diese Nebenwirkung als sehr selten angesehen. Bei häufig verabreichten Impfstoffen ergaben sich beispielsweise in der Auswertung einer großen US-amerikanischen Datenbank keine auffälligen Assoziationen (7). Als möglicher Pathomechanismus einer Vakzin-assoziierten Myokarditis kommt eine Arzneimittel-Hypersensitivität in Frage, die auch bei anderen Medikamenten auftreten kann, z.B. verschiedenen Antibiotika, Phenytoin, Clozapin (8).
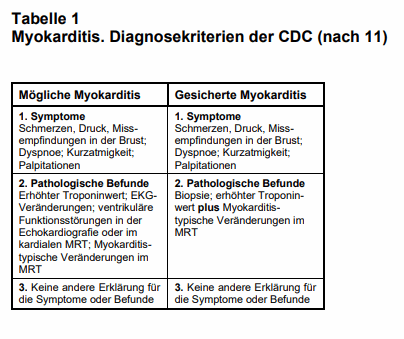
Im JAMA wurden jetzt zwei Berichte zur Myokarditis nach Impfung gegen SARS-CoV-2 veröffentlicht (9, 10). Myokarditiden, die bei Mitgliedern des US-amerikanischen Militärs nach der Impfung mit einem mRNA-Impfstoff zwischen Januar und April 2021 aufgetreten waren, wurden in einer Fallserie retrospektiv aufgearbeitet (9). Die Impfungen waren in 15 Regionen der USA durchgeführt worden, und die Nebenwirkung Myokarditis stützt sich auf Daten des VAERS. Suchkriterium war heftiger Brustschmerz, der nach einer Impfung gegen SARS-CoV-2 erstmalig aufgetreten war. Die CDC-Kriterien für die Diagnose Myokarditis sind in Tab. 1 aufgeführt (11).
Insgesamt wurden 23 männliche Soldaten im Alter vom 25-51 Jahren (Median 25 Jahre) identifiziert, bei denen innerhalb von 4 Tagen nach einer Impfung mit einem mRNA-SARS-CoV-2-Impfstoff akuter Brustschmerz aufgetreten war. Alle waren zuvor körperlich gesund und sehr fit. Sieben waren mit BNT162b2 (Tozinameran, Comirnaty®) und 16 mit mRNA-1273 (Moderna) geimpft worden. Die meisten Betroffenen (insgesamt 20) entwickelten die Symptome nach der 2. Impfung. Alle hatten ein deutlich erhöhtes Troponin (das 10-400fache der oberen Toleranzgrenze). Bei 19 Patienten fanden sich typische Veränderungen der ST-Strecken im EKG; bei 11 wurde eine Koronarangiografie durchgeführt und bei 5 ein Angio-CT, jeweils ohne pathologischen Befund. Vier Patienten hatten eine reduzierte linksventrikuläre Ejektionsfraktion (LVEF) von 40-50%. Bei 8 Betroffenen konnte die Diagnose im kardialen MRT bestätigt werden. Bei keinem Patienten gab es differenzialdiagnostisch Hinweise für COVID-19 oder andere Virus-Erkrankungen, akute Autoimmunerkrankung oder kardiale Ischämie (SARS-CoV-2-PCR-Test negativ bei 19). Alle Patienten hatten sich zum Zeitpunkt der Analyse bereits von der Erkrankung spontan erholt oder waren im Stadium der Rekonvaleszenz.
In der zweiten Recherche (10) wurde die Häufigkeit von Myokarditis am Duke University Medical Center in North Carolina in den 3 Monaten Februar bis April ausgewertet. Mit Beginn der Impfkampagne fanden sich 7 Patienten mit akuter Myokarditis, von denen 4 innerhalb der 5 Tage zuvor mit einem mRNA-Impfstoff geimpft worden waren: 3 junge Männer im Alter von 23-36 Jahren und eine 70jährige Frau. Zwei hatten ihre 2. Impfdosis mit mRNA-1273 erhalten und zwei BNT162b2. Alle hatten die Symptome einer Myokarditis sowie eine leicht eingeschränkte LVEF von 40-59%. Im Kardio-MRT wurde die Erkrankung bestätigt. Eine SARS-CoV-2-Infektion wurde akut und in der Anamnese ausgeschlossen, ebenso wie weitere Differenzialdiagnosen. Alle Patienten hatten sich im Verlauf von einer Woche erholt, die meisten unter Therapie mit Colchizin bzw. nichtsteroidalen Antirheumatika.
Im Einzugsbereich der Klinik waren bis Ende April 2021 insgesamt 561.000 Einwohner zweifach geimpft worden (33% der Bevölkerung). Die Inzidenz der Myokarditis ist mit 4 Betroffenen nach mRNA-Impfung gegenüber dem Vergleichszeitraum der Vorjahre zwar etwas erhöht, gemessen aber an der Zahl der verimpften Dosen sehr niedrig. Unklar ist, wie viele Geimpfte sich möglicherweise wegen geringer Symptome nicht in der Klinik vorgestellt haben.
Die beiden Artikel werden von zwei Editorials begleitet (12, 13), und es wird im Hinblick auf die Impfung von Kindern und Jugendlichen auf eine weitere online-Vorabveröffentlichung in Pediatrics hingewiesen: eine Fallbeschreibung von 7 männlichen US-amerikanischen Jugendlichen im Alter von 14-19 Jahren mit einer Myokarditis nach Impfung mit BNT162b2 (14). Auch hier bestand ein Zeitfenster von 4-5 Tagen von der Impfung bis zum Beginn der Symptome.
BNT162b2 ist seit Anfang Mai in den USA und seit Ende Mai durch die Europäische Kommission als einziger Impfstoff für Minderjährige > 12 Jahre zugelassen (vgl. 15). Moderna hat für seinen Impfstoff ebenfalls eine Zulassung für Kinder und Jugendliche beantragt. Bei Jugendlichen ist eine höhere systemische Reaktogenität und Immunogenität von BNT162b2 bekannt. Ob dies vermehrt zu Myokarditiden führt, ist unklar.
Auch das israelische Gesundheitsministerium berichtet über 121 Myokarditis-Fälle nach zweifacher Impfung von > 5 Mio. Geimpften (16). Das britische „Yellow-Card-System“ hat bis 23. Juni 2021 nach > 36 Mio. Impfungen insgesamt 60 Berichte über Myokarditis und 42 Berichte über Perikarditis nach Anwendung von BNT162b2 erhalten (17). Auch im Zusammenhang mit dem im UK wesentlich häufiger verimpften COVID-19-Impfstoff von AstraZeneca gab es 51 Berichte über Myokarditiden und 89 über Perikarditiden.
Wie bei den Sinusvenen-Thrombosen nach SARS-CoV-2-Vektorimpfstoffen (vgl. 18) fallen seltene Komplikationen in den Zulassungsstudien nicht auf. Umso wichtiger sind daher Systeme, die solche Meldungen jederzeit entgegennehmen, kontinuierlich auswerten und transparent veröffentlichen. Wir raten daher weiterhin, alle Verdachtsfälle auf Nebenwirkungen im Zusammenhang mit einer Impfung gegen SARS-CoV-2 an die zuständigen Stellen zu melden, einschließlich Fällen von COVID-19 nach Impfungen.
Fazit: Eine Hypersensitivitäts-Myokarditis nach Impfung mit SARS-CoV-2-mRNA-Impfstoffen ist eine seltene, aber schwerwiegende Komplikation. Sie tritt vermehrt bei jungen Männern auf und nach der 2. Impfdosis. Die Symptome beginnen meist innerhalb weniger Tage nach der Impfung. Der Verlauf scheint in den allermeisten Fällen mild zu sein. Ob Personen, die nach einem mRNA-Impfstoff gegen SARS-CoV-2 eine Myokarditis entwickelt haben, Auffrischimpfungen erhalten sollen – und wenn ja, mit welchem Impfstoff – ist noch völlig ungeklärt.
Literatur
- Tschöpe, C., et al.: Nat. Rev. Cardiol. 2021, 18, 169. Link zur Quelle
- Starekova, J., et al.: JAMA Cardiol. 2021. Published online January 14, e207444. Link zur Quelle
- Martinez, M.W., et al.: JAMA Cardiol. 2021. Published online March 4. e210565. Link zur Quelle
- Gargano, J.W., et al.: Link zur Quelle (Zugriff am 7.7.2021).
- Eckart, R.E., et al.: J. Am. Coll. Cardiol. 2004, 44, 201. Link zur Quelle
- Kim, Y.J., et al.: Acute Crit. Care 2019, 34, 165. Link zur Quelle
- Taliercio, C.P., et al.: Mayo Clin. Proc. 1985, 60, 463. Link zur Quelle
- Kuntz, J., et al.: Vaccine 2018, 36, 1524. Link zur Quelle
- Montgomery, J., et al.: JAMA Cardiol. Published online June 29. Link zur Quelle
- Kim, H.W., et al.: JAMA Cardiol. Published online June 29, 2021. Link zur Quelle
- https://www.cdc.gov/vaccines/acip/meetings/ downloads/slides-2021-06/02-COVID-Oster-508.pdf Link zur Quelle (Zugriff am 7.7.2021).
- Navar, A.M., et al.: JAMA Cardiol. Published online June 29, 2021. Link zur Quelle
- Shay, D.K., et al.: JAMA Cardiol. Published online June 29, 2021. Link zur Quelle
- Marshall, M., et al.: Pediatrics 2021. Published online June 4. Link zur Quelle
- AMB 2021, 55, 45. Link zur Quelle
- Surveillance of myocarditis. Israeli Ministry of Health; June 6, 2021: Link zur Quelle
- Coronavirus vaccine – weekly summary of Yellow Card reporting. Link zur Quelle (Zugriff am 7.7.2021).
- AMB 2021, 55, 36DB01. Link zur Quelle
- https://www.ema.europa.eu/en/news/meeting-highlights -pharmacovigilance-risk-assessment-committee- prac-5-8-july-2021 Link zur Quelle