Die Hemmung der Thrombozytenfunktion ist ein zentraler pharmakologischer Ansatzpunkt in der Behandlung arteriosklerotischer Gefäßerkrankungen. Aktivierte Thrombozyten sind nicht nur an der akuten Bildung von Blutgerinnseln, sondern auch maßgeblich bei der Entzündungsreaktion und bei der Heilung von Gefäßläsionen beteiligt. Somit hat die Hemmung der Thrombozytenfunktion nicht nur eine Bedeutung in der Prophylaxe thrombotischer Gefäßverschlüsse, sondern auch in der Prophylaxe entzündlicher und narbiger Stenosierungen, z.B. nach koronarer Ballondilatation.
Neben der bewährten und hochwirksamen Azetylsalizylsäure (ASS) sind in den vergangenen Jahren Substanzen entwickelt worden, die anders wirken und zum Teil noch effektiver sind als ASS. Diese Substanzen sind nicht nur als ein Ersatz bei Unverträglichkeit von ASS anzusehen. Da ASS die Thrombozytenaggregation auch in hohen Dosierungen nur unvollständig hemmt, ist in bestimmten Situationen eine Kombinationsbehandlung mit anderen Hemmstoffen sinnvoll.
Zum Verständnis der Funktionsweisen der Thrombozytenfunktionshemmer soll kurz und vereinfacht der Weg der Thrombozytenaktivierung erläutert werden (s. Abb. 1). Dieser Prozeß wird durch Aktivatorsubstanzen eingeleitet. Sie binden an Rezeptoren der Thrombozytenoberfläche. Die wichtigsten Aktivatoren sind: Thrombin, Kollagen, von Willebrand-Faktor, Thromboxan A2, ADP, Adrenalin, Vasopressin und Serotonin. Sie werden aus Läsionen der Gefäßwand, z.B. einem rupturierten Plaque, freigesetzt oder entstammen aus bereits aktivierten Thrombozyten. Nach Bindung an den Rezeptor werden Stoffwechselwege in den Thrombozyten aktiviert (Adenlylatzyklase, Proteinkinase A und C). Es resultieren drei wichtige intrazelluläre Veränderungen:
1. Es kommt zu Formänderungen des Zytoskeletts und der Oberfläche des Thrombozyten; er wird adhäsiv.
2. Aus den alpha-Granula werden Mediatoren freigesetzt. Dabei handelt es sich um entzündungs- und proliferationsfördernde Substanzen (PDGF, Serotonin, u.a.) und um thrombozytenaktivierende Faktoren (ADP, Thromboxan A2 u.a.).
3. Es kommt zu Änderungen der Konfiguration bzw. zur Expression von Membranrezeptoren, die der Thrombozytenadhäsion dienen (Glykoprotein GP Ib und GP IIb/IIIa).
Die ersten aktivierten Thrombozyten haften über ihren GP-Ib-Rezeptor an der Läsion der Gefäßwand. Die Verbindung wird über den von Willebrand-Faktor und über Fibronektin-Brücken hergestellt. An diesen ersten „Thrombozytenrasen“ lagern sich weitere aktivierte Thrombozyten an. Die Vernetzung dieser Thrombozyten erfolgt über den GP-IIb/IIIa-Rezeptor und Fibrinogen- bzw. von Willebrand-Faktor-Brücken. Schließlich entsteht ein stabiler weißer Thrombus.
Diese Prozesse lassen sich an verschieden Punkten pharmakologisch beeinflussen. ASS bewirkt über die Hemmung des Enzyms Zyklooxygenase (COX-1-Isoform) eine Verminderung der Thromboxan A2-Synthese. Dypiridamol hemmt die thrombozytäre Phosphodiesterase und damit die Adenylatzyklase-vermittelten intrazellulären Effekte. Trapidil wirkt auf die ADP- und Thromboxan-vermittelte Thrombozytenaktivierung und gefäßrelaxierend durch Stimulation der Prostazyklinsynthese. Sowohl für Dipyridamol als auch für Trapidil ist ein klinischer Nutzen belegt (s. AMB 1998, 32, 59; 84; 88b). Beide Substanzen haben aber keine große klinische Bedeutung erlangt, da ihre Vorteile gegenüber ASS marginal sind.
Trotz der in vielen Studien belegten effektiven Hemmung der Thrombozytenfunktion durch ASS bleiben die Blutplättchen prinzipiell weiter aggregationsfähig. Bei genügend hoher Konzentration von Aktivatorsubstanzen (ADP, Thrombin) kommt es auch unter ASS zur Plättchenaggregation und zur Thrombose. Daher ist eine Kombinationbehandlung mit anderen Thrombozytenfunktionshemmern oder Antithrombinen (Heparin, Hirudin) in besonders thrombogenen Situationen (instabile Angina pectoris, intrakoronare Interventionen) sinnvoll. In der Primär- und Sekundärprophylaxe arteriosklerotischer Erkrankungen bleibt ASS jedoch der Goldstandard (s. AMB 1993, 27, 41).
Die ADP-Rezeptor-Blocker Ticlopidin (Tiklyd) und Clopidogrel (Plavix) werden immer häufiger eingesetzt. Neben einer irreversiblen Hemmung der ADP-vermittelten Aktivierung des GP-IIb/IIIa-Rezeptors wird auch die Freisetzung der Mediatoren aus den alpha-Granula beeinflußt. Dadurch kann der sich selbst unterhaltende Aktivierungsprozeß der Thrombozyten unterbrochen werden. Die Wirkung tritt erst nach 2 Tagen ein, und das Wirkmaximum ist nach einer Woche erreicht. Clopidogrel ist etwa um den Faktor 5-7 mal wirksamer als die ältere Substanz Ticlopidin. In klinischen Studien zeigte sich unter Clopidogrel (1 mal 75 mg/d) bzw. Ticlopidin (2 mal 250 mg/d) ein leichter Vorteil gegenüber ASS (325 mg/d oder mehr) in der Sekundärprophylaxe nicht kardioembolischer Schlaganfälle. Nach den Daten der CAPRIE-Studie müssen 1000 Patienten nach Schlaganfall ein Jahr lang mit Clopidogrel behandelt werden, um 5 gravierende klinische Ereignisse (Tod, Reinsult, Myokardinfarkt) zu verhindern (s. AMB 1997, 31, 13a; 56b und 1998, 32, 84). Dabei ist offen, wie lange der ADP-Blocker verabreicht werden sollte. Da der Unterschied zwischen ASS und Clopidogrel bereits in den ersten Behandlungswochen sichtbar wurde und die Kaplan-Maier-Kurven später parallel verliefen, könnte eine passagere Therapie mit Clopidogrel möglicherweise den selben Nutzen bringen wie eine Langzeittherapie. Eine Verordnung von ADP-Blockern zur Sekundärprophylaxe des Schlaganfalls wird nach einer Kosten/Nutzen-Abwägung z.Z. auf einzelne Patienten beschränkt bleiben (s. AMB 1997, 31, 56b).
Eine wichtige Indikation für ADP-Blocker ist die Thromboseprophylaxe intrakoronarer Stents. Die 4-wöchige Kombinationstherapie mit 100 mg ASS/d plus 2 mal 250 mg Ticlopidin/d hat sich bewährt (s. AMB 1996, 30, 43). Wahrscheinlich ist sogar eine 2-wöchige Nachbehandlung mit ADP-Blockern ausreichend (2). Sehr wichtig ist es, bei elektiven Stent-Implantationen die Behandlung bereits 2 Tage vorher zu beginnen, da erst danach eine ausreichende Wirkung besteht. Studien mit Clopidogrel nach Stent-Implantation liegen noch nicht vor; es ist jedoch zu erwarten, daß ähnliche Effekte erzielt werden.
Beim Vergleich beider Substanzen schneidet Clopidogrel wegen der selteneren Nebenwirkungen günstiger ab. Nach Ticlopidin ist mit z.T. schwerwiegenden hämatologischen Komplikationen zu rechnen: Neutropenie (2,4%), Idiopathische thrombozytopenische Purpura, Hämolyse u.a. Daher sind engmaschige Blutbildkontrollen notwendig. Darüber hinaus treten häufig gastrointestinale (20% Diarrhö, Cholestase) und dermatologische (12% Exantheme) Nebenwirkungen auf. Bei Clopidogrel sind derartige Nebenwirkungen wesentlich seltener (Diarrhö 4,5%, Exantheme 6%, Neutropenie 0,2%). Blutungskomplikationen sind unter beiden Substanzen nicht häufiger als unter ASS. Ein weiterer Vorteil von Clopidogrel ist die tägliche Einmalgabe. Dafür ist Clopidogrel etwas teurer als Ticlopidin (5,69 DM vs. 4,99 DM/d).
Glykoprotein-IIb/IIIa-Rezeptor-Blocker sind die bisher wirksamsten Substanzen gegen aktivierte Thrombozyten. Die Entwicklungen innerhalb dieser Medikamentengruppe war in den vergangenen Jahren atemberaubend. Im Windschatten der explosionsartig zunehmenden koronaren Interventionen wurden innerhalb kürzester Zeit mehrere Substanzen zur Marktreife getrieben. Da aktivierte Thrombozyten beim akuten koronaren Ischämiesyndrom Dreh- und Angelpunkt für Entstehung und Unterhaltung thrombotischer und entzündlicher Prozesse sind, ist die vollständige Hemmung der Thrombozyten der wirksamste Eingriff. Durch die Besetzung/Blockade des GP-IIb/IIIa-Rezeptors wird die Vernetzung der Thrombozyten verhindert. Die Fähigkeit zum primären Verschluß von Wunden bleibt jedoch intakt, da dies über den GP-Ib-Rezeptor erfolgt.
Es gibt drei Gruppen von GP-IIb/IIIa-Rezeptor-Blockern (s.a. Tab. 1) :
1. Monoklonale Antikörper (Fab von c7E3): Abciximab (Reopro)
2. Niedermolekulare Peptide: Eptifibatid (Integrelin)
3. Peptidomimetika (Fibane):
a) parenterale: Tirofiban (Aggrastat), Lamifiban, Fradafiban
b) orale: Sibrafiban, Lefradafiban, Xemilofiban
Abciximab und Tirofiban sind in Deutschland zugelassen.
Aus den pharmakologischen Unterschieden der einzelnen Substanzen leitet sich die Differentialtherapie mit GP-IIb/IIIa-Rezeptor-Blockern ab. Der Antikörper Abciximab verdrängt auf Grund seiner hohen Rezeptoraffinität Fibrinogen aus einer bestehenden Rezeptorbindung und wirkt daher auch thrombolytisch. Das teure Abciximab wird z.Z. besonders dann im Herzkatheterlabor angewendet, wenn während der Interventionen thrombotische Komplikationen auftreten oder bei Interventionen mit hohem Risiko. Die Therapie mit den billigeren peptidischen und nichtpeptidischen GP-IIb/IIIa-Blockern läßt sich auf Grund der reversiblen Rezeptorbindung besser steuern, und mögliche Blutungskomplikationen sind einfacher zu beherrschen (Ausnahme orale Peptidomimetika). Daher bieten sich diese Mittel zur Gefäßbefriedung bei instabiler Angina pectoris an, da hier eine mehrtägige Therapie erforderlich sein kann. Tirofiban ist in Deutschland auch nur für die Indikation instabile Angina pectoris und Non-Q-Wave-Infarkt zugelassen. Die oralen GP-IIb/IIIa-Blocker sind zwar bequem zu applizieren; da sie jedoch sehr schlecht steuerbar sind, ist ihre zukünftige Rolle in der Therapie der akuten koronaren Ischämiesyndrome noch nicht klar.
Die klinischen Studien mit GP-IIb/IIIa-Rezeptor-Blockern können unter zwei Indikationen betrachtet werden: einerseits die Anwendung bei akuten koronaren Ischämiesyndromen (instabile Angina pectoris, Non-Q-Wave-Infarkt), andererseits die adjuvante Therapie bei koronaren Interventionen (elektive PTCA, Notfall- und Hochrisiko-PTCA). Eine Übersicht über die wichtigsten Studien gibt Tab. 2 (3-13).
Akute koronare Ischämiesyndrome und GP-IIb/IIIa-Rezeptor-Blockade: Es gilt heute als sicher, daß eine sofortige Koronarintervention bei instabiler Angina pectoris bzw. Non-Q-Wave-Infarkten wenig Vorteile bringt (14). Durch häufigere Komplikationen wirkt sich eine sofortige Intervention sogar nachteilig aus. Es wird daher vielerorts das Konzept der „medikamentösen Gefäßbefriedung“ verfolgt. Die Koronarangiographie erfolgt, wenn möglich, verzögert, d.h. nach medikamentöser Stabilisierung. Eine Intervention ist dann häufig nicht mehr notwendig.
Der Beitrag, den die GP-IIb/IIIa-Blocker zur Gefäßbefriedung leisten können, ist erheblich. Bei einer Metaanalyse der wichtigsten Studien zur Indikation „akutes koronares Ischämiesyndrom“ konnte zwar kein signifikanter Überlebensvorteil für die Behandelten errechnet werden. Allerdings fanden sich in allen Studien signifikant weniger koronare Ereignisse (Koronarintervention, Myokardinfarkt) wenn mit dem Verum behandelt worden war. Für den Endpunkt „Tod und nicht tödlicher Myokardinfarkt“ errechnete sich eine Odds Ratio von 0,8 nach 3 Tagen und 0,88 nach 30 Tagen bzw. 6 Monaten. Dies entspricht 16 verhinderten Ereignissen pro 1000 Behandlungen (15). Eine weitere wichtige Beobachtung aus diesen Studien war, daß, wenn eine Koronarintervention wegen medikamentös nicht mehr zu beherrschender Angina pectoris durchgeführt werden mußte, die mit Verum behandelten Patienten viel weniger Komplikationen erlebten, als die mit Plazebo behandelten.
Die zwischen den einzelnen Studien in Tab. 2 differierenden Ereignisraten sind vor allem durch Unterschiede in den Einschlußkriterien, Endpunktdefinitionen (z.B. Infarktdefinitionen an Hand der CKMB oder nach EKG) und durch die unterschiedlich häufigen Katheterinterventionen begründet.
Katheterinterventionen und GP-IIa/IIIb-Rezeptor-Blockade: In den Katheterinterventionsstudien ergab sich nach der erwähnten Metaanalyse kein Überlebensvorteil für die adjuvant mit GP-IIb/IIIa-Rezeptor-Blockern behandelten Patienten. Aber es fand sich ein deutlicher Vorteil hinsichtlich des kombinierten Endpunktes „nicht tödlicher Myokardinfarkt oder Tod“. Die Odds Ratio betrug nach 3 Tagen 0,57 (27 verhinderte Ereignisse auf 1000 Behandlungen) und nach 6 Monaten 0,76 (23/1000). Dabei wurden die besten Ergebnisse in den Abciximab-Studien erzielt.
Mußte bei Patienten mit instabiler Angina pectoris oder akuten Myokardinfarkt interveniert werden, dann waren unter GP-IIb/IIIa-Blockade die Komplikationen deutlich seltener als unter Heparin/ASS.
Besonders interessant sind auch die Daten aus der EPISTENT-Studie (16). Hier wurden 2400 Patienten vor geplanter Ballondilatation in drei Behandlungsarme randomisiert: 1. Ticlopidin plus Stent, 2. Abciximab plus alleinige PTCA, 3. Ticlopidin plus Abciximab plus Stent. Die letzte Gruppe schnitt mit 5,3% Komplikationen während 30 Tagen am günstigsten ab. Die Gruppe mit Ticlopidin plus Stent mit 10,8% am schlechteten. Überraschend war das gute Ergebnis in der Gruppe Abciximab plus PTCA. Mit 6,9% traten, obwohl kein Stent verwendet wurde, sehr wenige Komplikationen auf. Dies verleitete einige Befürworter der GP-IIb/IIIa-Blocker-Therapie schon dazu, das Ende den Stent-Implantationen einzuläuten. EPISTENT bestätigt, was schon in den Studien zu Interventionen bei akuten koronaren Ischämiesyndromen sichtbar wurde: durch die periinterventionelle GP-IIb/IIIa-Blockade können akute Thrombosen als Komplikation der PTCA sehr effektiv verhindert werden und damit wohl auch einige erneut notwendige PTCA und Stent-Implantationen.
Akuter Myokardinfarkt und GP-IIb/IIIa-Rezeptor-Blockade: Mit Abciximab konnten beim akutem Myokardinfarkt vergleichbare Wiedereröffnungsraten im Infarktgefäß erreicht werden wie mit Streptokinase. Daher lag es nahe, GP-IIb/IIIa-Rezeptor-Blocker mit einem Thrombolytikum zu kombinieren. Tatsächlich ließen sich in den ersten Studien mit einer solchen Kombinationsbehandlung die Infarktgefäße häufiger wiedereröffnen als mit dem Thrombolytikum alleine, allerdings zum Preis vermehrter Blutungskomplikationen (Tab. 2). Weitere Studien mit reduzierten Dosen werden folgen. Ziel ist es, daß es mit der Kombinationstherapie Fibrinolyse plus GP-IIb/IIIa-Blockade gleich häufig gelingt, die verschlossenen Koronararterien wiederzueröffnen, wie mit der Akut-PTCA. Damit stünde eine sehr wirksame Therapie prinzipiell jederzeit und überall zur Verfügung.
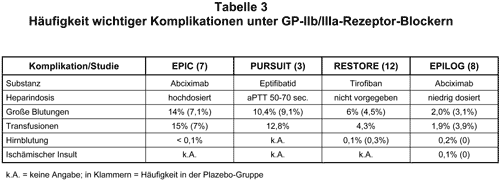
Komplikationen unter Therapie mit GP-IIb/IIIa-Rezeptor-Blockern: Die häufigsten Komplikationen bei der Anwendung von GP-IIb/IIIa-Rezeptor-Blockern sind Blutungen. Zu bedrohlichen Blutungen kam es in den Studien bei maximal 14% der Patienten (Tab. 3), wobei ältere Menschen häufiger betroffen waren. Später ist klar geworden, daß Häufigkeit und Schwere der Blutungen nicht alleine von der Dosierung des GP-IIb/IIIa-Blockers abhängen, sondern besonders von der adjunktiven Heparindosierung. Bei reduzierter Heparindosis (doppelte aPTT) ist die Anwendung relativ sicher. Eine Gabe ganz ohne Heparin wird nicht empfohlen.
Tritt eine bedrohliche Blutung auf, muß die Infusion des GP-IIb/IIIa-Rezeptor-Blockers und von Heparin beendet werden. Da durch Abciximab der Rezeptor dauerhaft blockiert ist, wird hier die Gabe von Thrombozyten Mittel der Wahl sein. Die zugeführten Thrombozyten bleibenen größtenteils funktionstüchtig, da die Plasmahalbwertszeit von Abciximab nur wenige Minuten beträgt und die Antikörper nur in geringem Ausmaß zwischen den Thrombozyten ausgetauscht werden.
Bei den peptidischen und peptidomimetischen Rezeptor-Blockern erholt sich wegen der reversiblen Rezeptorbindung die Thrombozytenfunktion innerhalb weniger Stunden nach Abstellen der Infusion. Die Gabe von Thrombozytenkonzentraten ist in den ersten Stunden nicht sehr wirksam, da die zugeführten Plättchen durch den noch mehrere Stunden im Plasma zirkulierenden Wirkstoff inaktiviert werden.
Die oralen GP-IIb/IIIa-Blocker haben eine besonders lange Bioverfügbarkeit. Daher ist das Stillen von Blutungen in diesem Fall besonders schwierig. Substituierte Thrombozyten werden wegen der langen Halbwertszeit rasch inaktiviert. Daher können in gefährlichen Situationen Magenspülung, Gabe von Aktivkohle, forcierte Diurese und Ultrafiltration angezeigt sein.
Die Häufigkeit hämorrhagischer oder ischämischer Schlaganfälle war überraschenderweise unter GP-IIb/IIIa-Blockern in den publizierten Studien nicht erhöht (Tab. 3).
Um Blutungen zu vermeiden, gelten für GP-IIb/IIIa-Blocker ähnliche Kontraindikationen wie für Thrombolytika. Bei schwerer Leberinsuffizienz und gestörter Blutgerinnung (INR > 1,5; Thrombozyten < 90000/µl) dürfen die Substanzen nicht angewendet. Bei schwerer Niereninsuffizienz (Kreatinin-Clearance < 30ml/min) muß die Dosis reduziert werden. Bei 0,5-1,6% der Behandlungen wird eine reversible Thrombozytopenie (< 50000/µl) beobachtet. Daher müssen neben der Blutgerinnung auch die Thrombozytenzahlen engmaschig überwacht werden. Ist bei einem Patienten schon einmal eine Thrombopenie unter GP-IIb/IIIa-Blockern aufgetreten, sollte keine Reexposition erfolgen. Über Allergien als Nebenwirkungen gibt es noch wenig Informationen. Es muß jedoch davon ausgegangen werden, daß inaktivierende Antikörper und/oder systemische Reaktionen prinzipiell auftreten können, besonders bei den eiweißhaltigen Präparaten. Andere mögliche Nebenwirkungen sind Fieber, Übelkeit und Kopfschmerzen (jeweils < 2% der Patienten). Fazit: Die ADP-Blocker Ticlopidin und Clopidogrel und die GP-IIb/IIIa-Rezeptor-Blocker Abciximab, Tirofiban und Lamifiban hemmen die Thrombozytenaggregation stärker als ASS. Die Wirksamkeit dieser Substanzen ist in vielen klinischen Studien eindeutig belegt. Diese neuen Thrombozytenfunktionshemmer sind für kardiologische und angiologische Indikationen ein Gewinn. Die Indikationen sind jedoch noch nicht endgültig geklärt und eng zu stellen, da diese reißerisch und pharmakodynamisch inkorrekt als „Superaspirine“ gepriesenen Substanzen nicht nur erheblich teurer, sondern auch gefährlicher sind als ASS.
Literatur
1. Alexander, J.H., et al.: Curr. Opin. Cardiol. 1998, 12, 427.
2. Berger, P.B., et al.: Circulation 1999, 99, 248.
3. PURSUIT = Platelet glycoprotein IIb/IIIa in Unstable angina: Receptor Suppression Using Integrilin Therapy: N. Engl. J. Med. 1998, 339, 436.
4. PRISM = Platelet Receptor inhibition in Ischemic Syndrome Management: N. Engl. J. Med. 1998, 338, 1498.
5. PRISM PLUS = Platelet Receptor inhibition in Ischemic Syndrome Management in Patients Limited by Unstable Signs and symptoms: N. Engl. J. Med. 1998, 338, 1488.
6. PARAGON = Platalet IIb/IIIa Antagonist for the Reduction of Acute coronary syndrome events in a Global Organisation Network: Circulation 1998, 97, 2386.
7. EPIC = Evaluation of 7E3 for the Prevention of Ischemic Complications: N. Engl. J. Med. 1994, 330, 956.
8. EPILOG = Evaluation in PTCA to Improve Long-term Outcome with abciximab GP IIb/IIIa Blockade: N. Engl. J. Med. 1997, 336, 1689.
9. CAPTURE = C7E3 Fab Antiplatelet Therapy in Unstable Refractory Angina: Lancet 1997, 349, 1429.
10. RAPPORT = ReoPro in Acute myocardial infarction and Primary PTCA Organization and Randomized Trial: Circulation 1997, 96, I-473.
11. IMPACT II = Integrilin to Minimise Platelet Aggregation and Coronary Thrombosis II: Lancet 1997, 349, 1422.
12. RESTORE = Randomized Efficacy Study of Tirofiban for Outcomes and REstenosis: Circulation 1997, 96, 1445.
13. TIMI 14 = Thrombolysis In Myocardial Infarction 14: J. Am. Coll. Cardiol. 1998, 31 Suppl., A-191.
14. VANQWISH = Veterans Affairs Non-Q–Wave Infarction Strategies in Hospital trial: N. Engl. J. Med. 1998, 338, 1785.
15. Kong, D.F., et al.: Circulation 1998, 98, 2829.
16. EPISTENT = Evaluation of Platelet IIb/IIIa Inhibitor for Stenting: Lancet 1998, 352, 87.