Herzinfarkt und Schlaganfall sind eine wichtige Ursache erhöhter Letalität in der perioperativen Phase. Schwankungen des Blutdrucks, Herzrhythmusstörungen und Änderungen der Thrombozytenaggregation sind u.a. dafür verantwortlich. Daher wurde die prophylaktische Wirksamkeit von Betablockern und auch von ASS in zahlreichen Studien und Metaanalysen untersucht. DER ARZNEIMITTELBRIEF hat mehrfach darüber berichtet (1-3). Betablocker senken möglicherweise die Infarktrate, aber nicht die Letalität. Clonidin dämpft ebenfalls den Sympathikotonus, aber eine prophylaktische Wirkung wurde nur nach kardialen Operationen in kleineren Studien nachgewiesen. Die Indikation zur perioperativen Hemmung der Thrombozytenaggregation folgt Regeln, die sich am CHA2DS2-VASc-Score (vgl. 4) und dem intraoperativen Blutungsrisiko der Patienten orientieren (vgl. 3). Aber auch für dieses Konzept gibt es keine überzeugende Bestätigung. Nun wurden in zwei Publikationen aus Kanada klinisch wichtige Ergebnisse einer großen multinationalen, randomisierten Studie mitgeteilt zur perioperativen Prophylaxe mit Clonidin bzw. ASS bei nicht-kardialen Operationen (5, 6).
Methodik: In 135 Zentren in 23 Ländern wurden insgesamt 10.010 Patienten (Alter 68,5 ± 10,4 Jahre; 52,6% Männer) mit erhöhtem kardiovaskulärem Risiko eingeschlossen. Sie mussten mindestens zwei Punkte im CHA2DS2-Vasc-Score haben. Ausgeschlossen wurden antihypertensiv behandelte Patienten und solche mit Zustand nach hämorrhagischem Insult oder nach Implantation eines koronaren Stents – d.h. mit klarer Indikation für oder gegen die zu untersuchende Prophylaxe. Die Patienten wurden 1:1:1:1 randomisiert und erhielten verblindet eine Doppelmedikation (2×2 factorial design) und zwar entweder 1. Clonidin (0,2 mg/d) plus ASS (100 mg/d) oder 2. Clonidin plus ASS-Plazebo oder 3. Clonidin-Plazebo plus ASS oder 4. Clonidin-Plazebo plus ASS-Plazebo. So konnten die Ergebnisse jedes Patienten entsprechend den medikamentösen Kombinationspartnern zweimal gezählt und zwei Wirkstoffe gleichzeitig und plazebokontrolliert mit hoher Fallzahl untersucht werden. Die Patienten erhielten die Studienmedikation (s.o.) bei nicht-kardialen Operationen unmittelbar präoperativ sowie über drei Tage postoperativ und wurden 30 Tage nachbeobachtet. Kombinierter primärer Endpunkt war: Tod oder nicht-tödlicher Herzinfarkt; sekundäre Endpunkte: zusätzlich nicht-tödlicher Schlaganfall sowie zusätzlich kardiale Revaskularisation, nicht-tödliche Lungenembolie oder nicht-tödliche Beinvenenthrombose; zu den zahlreichen tertiären Endpunkten gehörten: Rehospitalisation wegen einer kardiovaskulären Erkrankung, Vorhofflimmern, Amputationen sowie Niereninsuffizienz mit Dialysepflichtigkeit.
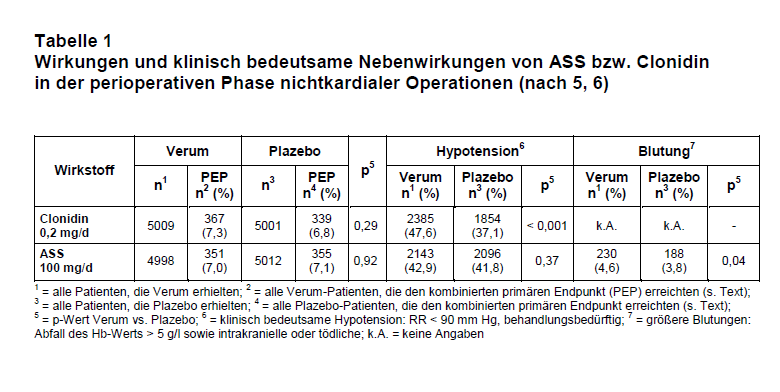
Ergebnisse: Weder die Propylaxe mit Clonidin noch mit ASS senkte die Letalität oder die Häufigkeit von Herzinfarkten 30 Tage nach einer nicht-kardialen Operation. Die Häufigkeit war bei Clonidin und Clonidin-Plazebo sowie ASS und ASS-Plazebo etwa 7% (vgl. Tab. 1). Auch die Häufigkeit von Schlaganfällen sowie des zweiten und des dritten Endpunkts wurde statistisch nicht beeinflusst. Demgegenüber gab es eine hochsignifikante Zunahme von bedrohlichen Hypotensionen (und Bradykardien) bei Clonidin und massive Blutungen bei ASS (vgl. Tab. 1).
Diskussion: In dieser Untersuchung wurde weder mit ASS noch mit Clonidin ein positiver Effekt gesehen. Es ist erstaunlich, dass ein negativer Befund überhaupt im N. Engl. J. Med. so ausführlich veröffentlicht wurde. Bei Patienten mit erhöhtem kardiovaskulärem Risiko ist die Wirksamkeit einer niedrig dosierten ASS-Prophylaxe insgesamt evident (vgl. 7). In der perioperativen Phase ist das offenbar anders und auf den ersten Blick nicht plausibel. Jedoch wird das Risikoprofil und auch die Häufigkeit erwünschter und unerwünschter Arzneimittelwirkungen und -wechselwirkungen offenbar massiv verändert durch: Angst, Schmerzen, gesteigerten Sympathikotonus mit Tachykardie und Hypertonie, gesteigerten Vagotonus mit Bradykardie, Volumenmangel mit Hypotension, Abnahme des Herzzeitvolumens, Azidose und Hypoxämie. Clonidin mindert den Sympathikotonus, sowie Angst und Unruhe, führt aber oft zu bedrohlichen Hypotensionen und bradykarden Rhythmusstörungen und auf diese Weise ggf. zu Durchblutungsstörungen und Infarkten. ASS verhindert möglicherweise auch postoperativ Infarkte, andererseits induziert es aber im perioperativen Stress mehr Blutungen mit Hypotensionen, die wiederum zu Infarkten führen und so den Nutzen aufheben können.
Dass sich postoperativ pharmakodynamische Wirkungen ändern, bezeichnen die Autoren des Editorials (8) im selben Heft des N. Engl. J. Med. als „The Yin and Yang of perioperative medicine“. In diesem Zusammenhang ist damit gemeint: Arzneimittel ergänzen, beeinflussen oder antagonisieren sich in der perioperativen Phase anders als sonst. Ein Fortschritt bei der Risikoreduktion – speziell für Herzinfarkt – sei nur dann möglich, wenn es gelänge, Arzneimittel zu entwickeln, bei denen auch in Situationen mit pathophysiologischen Besonderheiten die Nebenwirkungen (Yang) nicht die positiven Wirkungen (Yin) mindern oder aufheben. Dies gilt allerdings nicht nur für die perioperative Pharmakotherapie, sondern ist immer und überall das Ziel des Fortschritts.
Fazit: In der POISE-2-Studie wurde bei > 10.000 Patienten in 135 Zentren und 23 Ländern mit komplexer Methodik untersucht, ob ASS oder Clonidin postoperativ eine prophylaktische Wirkung hinsichtlich vaskulärer Erkrankungen haben und die Letalität senken. Das Ergebnis ist eindeutig negativ, denn beide Wirkstoffe senken weder die Letalität noch die Häufigkeit von Herzinfarkten, steigern aber hochsignifikant die Blutungsrate (ASS) bzw. die Zahl von Hypotensionen und Bradykardien (Clonidin). Beide Wirkstoffe sollten daher in der perioperativen Phase nicht eingenommen bzw. abgesetzt werden. Ausnahme: Patienten mit intrakoronaren Stents. Dazu müssen zusätzliche Informationen abgewartet werden.
Literatur
- Devereaux,P.J., et al. (POISE = PeriOperative ISchemic Evaluation):Lancet 2008, 371, 1839 Link zur Quelle . Vgl. AMB 2008, 42, 54. Link zur Quelle
- AMB2013, 47, 75. Link zur Quelle
- AMB2010, 44, 17. Link zur Quelle
- AMB2014, 48, 35. Link zur Quelle
- Devereaux,P.J., et al. (POISE-2 = PeriOperative ISchemic Evaluation2): N. Engl. J. Med. 2014, 370, 1494. Link zur Quelle
- Devereaux,P.J., et al. (POISE-2 = PeriOperative ISchemic Evaluation2): N. Engl. J. Med. 2014, 370, 1504. Link zur Quelle
- AntithromboticTrialists’ Collaboration: Brit. Med. J. 2002, 324, 71. Erratum: Brit.Med. J. 2002, 324, 141. Link zur Quelle
- Vaishnava, P., und Eagle, K.A.: N. Engl. J. Med.2014, 370, 1554. Link zur Quelle