Ob auch ältere Menschen zur Prävention kardiovaskulärer Ereignisse Statine einnehmen sollten und wenn ja, bis zu welchem Alter, wird immer wieder kontrovers diskutiert. Das liegt u.a. daran, dass in den meisten randomisierten kontrollierten Studien (RCT) der Anteil der Patienten > 75 Jahre sehr gering war bzw. dass diese erst gar nicht in die Studien eingeschlossen wurden, obwohl sie ja einen wesentlichen Teil der Zielgruppe ausmachen. Wir hatten kürzlich über Register-Daten aus Spanien berichtet, die gezeigt haben, dass eine Primärprävention mit Statinen bei Menschen > 75 Jahre ohne Typ-2-Diabetes unterbleiben sollte, da sie kardiovaskuläre Ereignisse und Letalität nicht reduziert (1). Es gibt bis heute nur ein RCT, das die Wirksamkeit von Statinen speziell bei älteren Patienten getestet hat. In der PROSPER-Studie waren 9% der Studienteilnehmer zwischen 65-70 Jahre alt, und bei 51% lag das Alter zwischen 70-75 Jahre und bei 41% > 75 Jahre (2). Der primäre Endpunkt (kombinierter Endpunkt: Todesfälle infolge Koronarer Herzkrankheit (KHK), nicht-tödlicher Herzinfarkt und Schlaganfall) wurde nach durchschnittlich 3,2 Jahren mit Pravastatin gegenüber Plazebo um 2,1% reduziert (14,1% vs. 16,2%; vgl. 3). Die Studie wurde allerdings im Jahr 1997 begonnen und entspricht nicht mehr der heutigen Behandlungsrealität. Derzeit läuft ein australisches RCT mit dem Akronym STAREE, in dem Atorvastatin vs. Plazebo in der Primärprävention bei gesunden Menschen > 70 Jahre getestet wird (4). Studienendpunkte sind neben kardiovaskulären Ereignissen auch neu auftretende Behinderungen sowie Demenz. Ziel ist es, 18.000 Patienten einzuschließen; erste Ergebnisse werden Ende 2022 erwartet. Bis dahin müssen wir unsere Therapieentscheidung hinsichtlich Verordnung von Statinen an den Studienergebnissen orientieren, die publiziert sind.
Die Cholesterol Treatments Trialists’ (CTT) Collaboration ist eine internationale Gruppe, die periodisch Metaanalysen von großen und langfristigen RCT zu lipidsenkenden Therapien durchführt (5). Die Collaboration wurde 1994 gegründet und wird durch öffentliche Gelder finanziert. Sie hat Zugriff auf die Daten von 187.000 Patienten aus 28 RCT mit Statinen. In 23 RCT wurden Statine mit Plazebo bzw. „usual care“ und in 5 RCT eine Statin-Behandlung in hoher Dosis vs. Standard-Dosis verglichen. Nun wurde im Lancet eine Metaanalyse dieser Daten zu den Behandlungseffekten von Statinen in Abhängigkeit vom Lebensalter publiziert (6). Es wurde die relative Risikominderung für vaskuläre Ereignisse durch eine Statin-Behandlung in 6 Altersgruppen berechnet (≤ 55; 56-60; 61-65; 66-70; 71-75 und > 75 Jahre). 14.500 Studienteilnehmer (8% aller) waren zu Studienbeginn > 75 Jahre alt.
Ergebnisse: Die mediane Nachbeobachtung in der Metaanalyse betrug knapp 5 Jahre. Die > 75-Jährigen waren im Mittel 78,8 Jahre alt. 55% erhielten das Statin wegen einer manifesten KHK, die übrigen wohl zur Primärprävention. Über alle Altersklassen und Indikationen führte die Statin-Behandlung pro mmol/l LDL-Senkung (entsprechend 38 mg/dl) zu einer relativen Reduktion des Risikos (RR) für ein klinisch bedeutsames vaskuläres Ereignis (Primärer kombinierter Endpunkt: klinisches KHK-Ereignis, koronare Revaskularisation oder Schlaganfall) von 21% pro Jahr Behandlung. Ein Nutzen wurde in allen fünf untersuchten Altersgruppen gefunden. Die Effektstärke nimmt jedoch mit zunehmendem Alter ab: bei den ≤ 55-Jährigen beträgt die Risikoreduktion pro mmol LDL-C-Senkung 25% (RR: 0,75; 95%-Konfidenzintervall = CI: 0,70-0,81) und bei den > 75-Jährigen 13% (RR: 0,87; CI: 0,77-0,99). Nach Ausschluss von 4 RCT, in denen Statine bei Patienten mit chronischer Herzinsuffizienz oder dialysepflichtiger Niereninsuffizienz getestet wurden – bei diesen Patienten ist kein Nutzen nachgewiesen (7) – beträgt die Risikoreduktion bei den > 75-Jährigen pro mmol LDL-Senkung 19% (RR: 0,81; CI: 0,66-0,99).
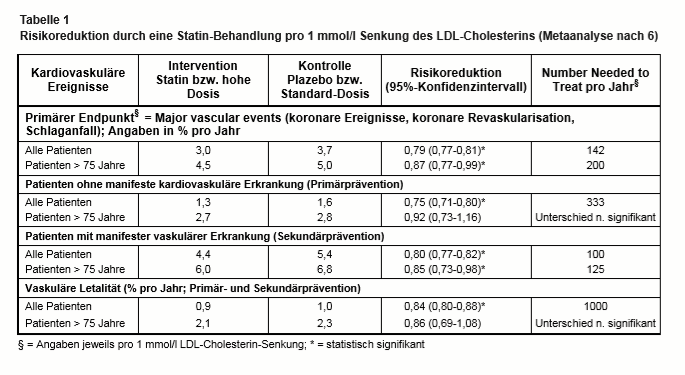
Der Nutzen bei den > 75-Jährigen ist jedoch nur in der Sekundärprävention (RR: 0,74), nicht in der Primärprävention (RR: 0,92) nachweisbar, und Todesfälle werden bei 1 mmol/l LDL-Senkung nicht verhindert (RR: 0,95; CI: 0,83-1,07; s. Tab. 1). Gelingt mit Statinen eine LDL-Senkung um 2 mmol/l (65 mg/dl), dann verdoppeln sich die berechneten Effektstärken. Dies erfordert jedoch eine Hochdosis-Statin-Behandlung, die bei älteren Patienten oft an den Nebenwirkungen und/oder Wechselwirkungen scheitert. Auf dieses Problem weisen auch die beiden Kommentatoren der Metaanalyse hin (8). Wegen Multimorbidität, Multimedikation und vermehrter Anfälligkeit für Nebenwirkungen setzten ältere Menschen die Statine häufig ab. Die in die Metaanalyse eingegangenen älteren Studienpatienten seien zudem stark selektiert, mit geringer Komorbidität, weniger Begleitmedikation und wahrscheinlich hoher Motivation und Adhärenz. Daher sei eine Verallgemeinerung auf alle älteren Menschen generell problematisch. Auch habe sich das Management der häufigsten Komorbiditäten in den letzten Jahren erheblich gewandelt. Daher sei es denkbar, dass die gleichen Studien heute zu geringeren Effekten führen.
Fazit: Die Behandlung mit Statinen reduziert auch bei Menschen > 75 Jahren signifikant die kardiovaskuläre Mortalität (insgesamt -13% pro Jahr und mmol/l LDL-C-Senkung), nicht aber die Letalität. Der Nutzen in der Primärprävention ist minimal und bei Patienten mit Herz- und terminaler Niereninsuffizienz nicht nachweisbar. In der Sekundärprävention sind Statine dagegen auch bei älteren Menschen empfehlenswert – vorausgesetzt, ihnen wird der Nutzen gut erklärt und sie vertragen Statine bzw. nehmen sie auch regelmäßig ein (Adhärenz).
Literatur
- AMB 2018, 52, 77. Link zur Quelle
- Shepherd, J., et al. (PROSPER = PROspective Study of Pravastatin in the Elderly at Risk): Lancet 2002, 360, 1623. Link zur Quelle
- AMB 2002, 36, 91 Link zur Quelle . AMB 2003, 37, 15b. Link zur Quelle
- STAREE = A clinical trial of STAtin therapy for Reducing Events in the Elderly: ClinicalTrials.gov. NCT02099123.
- https://www.cttcollaboration.org/ Link zur Quelle
- CTT = Cholesterol Treatment Trialists’ collaboration: Lancet 2019, 393, 407. Link zur Quelle
- Catapano, A.L., et al.: Eur. Heart J. 2016, 37, 2999. Link zur Quelle
- Cheung, B.M.Y., und Lam, K.S.L.: Lancet 2019, 393, 379. Link zur Quelle