Zusammenfassung
Eine aktualisierte Cochrane-Metaanalyse von 319 Studien zur Tabakentwöhnung zeigte, dass Nikotin-haltige elektronische Zigaretten sowie Vareniclin und Cytisin in etwa gleichem Ausmaß am wirksamsten waren. Der absolute Erfolg ist allerdings bescheiden: Von 100 Zigarettenrauchern waren im Mittel 14 für mindestens 6 Monate abstinent. Bupropion, Nikotinpflaster und schnell wirkende Nikotinersatz-Therapien waren ebenfalls wirksamer als Plazebo oder keine Intervention; die Kombination von Nikotinpflaster mit schnell wirkenden Nikotinersatz-Therapien war aber ähnlich erfolgreich wie die wirksamsten Strategien. Das Ausschleichen von Nikotin und Nikotin-freie elektronische Zigaretten sind dagegen weitgehend unwirksam. Das gesundheitliche Langzeitrisiko Nikotin-haltiger elektronischer Zigaretten ist noch nicht bekannt. Die Wahl bei Medikamenten zur Tabakentwöhnung ist wegen anhaltender Lieferschwierigkeiten eingeschränkt.
Viele Menschen rauchen, und viele von ihnen möchten gerne damit aufhören. Doch das ist sehr schwierig. Keith Richards und Lou Reed sollen laut einem Bericht im Musikmagazin „Rolling Stone“ zu dem Schluss gekommen sein, dass es schwieriger ist, mit Nikotin aufzuhören als mit Heroin.
Inhaliertes Nikotin bindet an den nikotinischen Acetylcholinrezeptor und setzt Dopamin und Noradrenalin sowie psychotrope Neurotransmitter frei, die mit „Glücksgefühlen“ assoziiert sind. Ein Abfall der Dopamin- und Noradrenalin-Konzentration führt zu systemischen Entzugserscheinungen und Suchtverhalten [1]. Selbst bei schweren gesundheitlichen Schäden können viele nicht vom Rauchen lassen.
Tabakrauchen ist durch die regelmäßige Inhalation von karzinogenen, teratogenen und atherogenen Schadstoffen der weltweit führende, vermeidbare Risikofaktor für Krankheit und Tod. Investitionen in die Tabakentwöhnung (TE) werden unter gesundheitsökonomischen Aspekten als eine sehr kosteneffektive Maßnahme im gesamten Gesundheitswesen eingestuft [2]; 30. November 2021.“ link=“www.nice.org.uk/guidance/ng209 2021″].
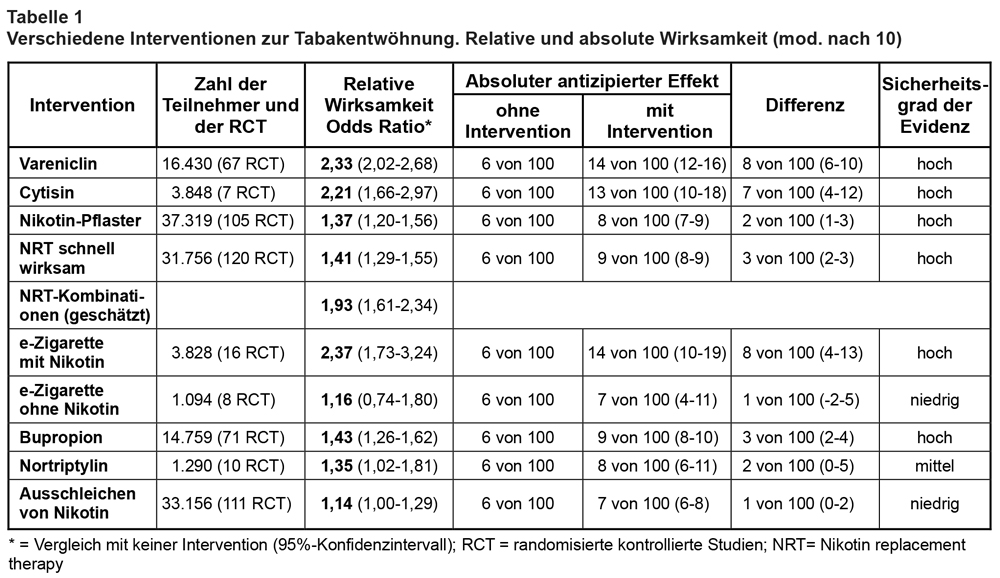
Die Erfolgsquote bei der TE ist allerdings enttäuschend: aus eigenem Antrieb erreichen nur 6% eine Abstinenz über 6 Monate (s. Tab. 1). Als ein mehr Erfolg versprechendes Konzept wird eine Kombination aus verhaltens- bzw. psychotherapeutischer Kleingruppentherapie (Einüben alternativer Verhaltensweisen zum Rauchen und Entspannungstechniken) plus Medikamenten gegen Entzugssymptome angesehen [3]. Hierfür stehen retardierte und für das „Craving“ schnell wirksame Präparate zur Verfügung.
Nikotinersatz-Präparate („Nicotine replacement therapy“ = NRT): Nikotin-Pflaster sorgen für gleichmäßige Blutspiegel: Über 16 bzw. 24 Stunden wird etwa ein Milligramm Nikotin pro Stunde freigesetzt. Für die Bedarfstherapie kann mit Lutsch- oder Sublingual-Tabletten, Kaugummi, Mund- oder Nasenspray die Dosierung von Nikotin individuell angepasst werden (vgl. [4]). Bei unzureichender Wirksamkeit einer Monotherapie empfiehlt die S3-Leitlinie zur Tabakentwöhnung von 2020 [5] eine Zweifach-Kombination aus Pflaster plus einer schnell wirksamen NRT.
Partielle Nikotinrezeptor-Agonisten: Vareniclin (Champix®) und Cytisin (Asmoken®) binden wie Nikotin an den Alpha4-Beta2-Acetylcholinrezeptor, der maßgebend ist für die Entwicklung einer Nikotinabhängigkeit. Durch die agonistische Wirkung wird der Rezeptor stimuliert und dadurch das Verlangen nach der nächsten Zigarette reduziert. Inhaliertes Nikotin kann dann nicht mehr an den besetzten Rezeptor binden, und die Sekretion von psychotropem Dopamin bleibt aus [6]. Dieser partielle Antagonismus in Gegenwart von Nikotin unterbindet den belohnenden und verstärkenden Effekt des Rauchens. Die Wirkung ist zwar schwächer als die von Nikotin, reicht aber aus, um das Rauchverlangen zu mildern. Cytisin, ein Alkaloid des Goldregens, gilt als pflanzliches Vorbild von Vareniclin und wurde früher, v.a. in Osteuropa, zu TE eingesetzt. Es wird in Deutschland und Österreich unter dem insinuierenden Namen Asmoken® vertrieben, ist derzeit aber nicht lieferbar. Sein Nutzen wird noch erforscht [7].
Antidepressiva: Bupropion (Elontril®, Wellbutrin® u.a.) ist als Antidepressivum etabliert [8]; sein Wirkmechanismus bei der TE ist noch nicht vollständig geklärt. Bupropion erhöht als selektiver Dopamin- und Noradrenalin-Wiederaufnahme-Hemmer die Konzentration dieser Neurotransmitter im Gehirn und kann nikotinbedingte Entzugssymptome und Rauchverlangen mildern (vgl. [4]). Patienten nehmen unter Bupropion-Therapie weniger stark an Gewicht zu als unter einer Behandlung mit Plazebo, was von Entwöhnungswilligen als positiver Nebeneffekt geschätzt wird.
Nortriptylin ist ein Serotonin- und Noradrenalin-Wiederaufnahmehemmer (SNRI). Für die Indikation TE ist es weltweit nur in Neuseeland zugelassen. Die Leitlinie zur TE zitiert: „Nortriptylin kann zur Tabakentwöhnung unter Beachtung möglicher Risiken angeboten werden, wenn zugelassene Therapieformen nicht zum Erfolg geführt haben“ [5]. Warum Bupropion und Nortriptylin offenbar die einzigen Antidepressiva mit TE-Potenzial sind, ist nicht klar. Vermutlich ist ihre Wirkung stärker durch nikotinerge „pathways“ geprägt als andere Antidepressiva.
Vareniclin, über dessen Wirkungen und Nebenwirkungen bei der TE wir bereits ausführlich berichtet haben (vgl. [4], [9]), ist wegen Verunreinigungen mit Nitrosaminen im Herstellungsprozess nicht lieferbar; auch Cytisin nicht, so dass neben der NRT in Deutschland und Österreich derzeit nur Bupropion zur TE zur Verfügung steht. Zu beachten ist, dass für eine optimale Wirkung mit der Einnahme bereits zwei Wochen vor dem festgelegten Rauchstopp begonnen und in aufsteigender Dosierung verordnet werden muss. Antidepressiva, wie auch NRT, sollten in der Regel nicht länger als zwei, ggf. drei Monate in dieser Indikation eingesetzt werden.
Die elektronische Zigarette (e-Z) gibt es seit 2006 auf dem europäischen Markt; sie wird zunehmend auch zur TE propagiert und angewendet. Eine nikotinhaltige, aromatisierte Flüssigkeit wird ohne einen Verbrennungsprozess verdampft, sog. „Vaping“ [10]. Als Träger dienen Propylenglycol und Glycerol. Während die derzeit gültige S3-Leitlinie zur TE [5] noch zurückhaltend formuliert: „Die Befundlage hinsichtlich Wirkung und Risiken der E-Zigarette in der Tabakentwöhnung ist uneinheitlich, mit Hinweisen auf ein Entwöhnungspotenzial und auf langfristige Risiken dieser neuen Produkte“, wird das Potenzial der e-Z als Entwöhnungsoption in Studien zunehmend bestätigt [8], [11].
Um Nutzen und Risken der einzelnen Entzugsmethoden, einschließlich der e-Z, zu evaluieren, wurden in einem aktuellen Cochrane Review alle bis zum 29.4.2022 verfügbaren randomisierten kontrollierten Studien (RCT) zur TE herangezogen und die Methoden in einer Netzwerk-Metaanalyse miteinander verglichen [12].
Studiendesign: Insgesamt erfüllten 319 RCT die Kriterien für die Metaanalyse. In 835 Studienarmen waren weltweit 157.179 erwachsene Probanden eingeschlossen und über mindestens 6 Monate nachbeobachtet worden. Dabei kamen folgende Verfahren zum Einsatz: NRT in Form lang und schnell wirkender Zubereitungen, Vareniclin, Cytisin, Bupropion, Nortriptylin, orale Plazebos, keine Medikation, Nikotin enthaltende e-Z (Ne-Z) und Nikotin-freie e-Z (Nfe-Z). Studien mit Schwangeren oder solche mit e-Z, die in irgendeiner Weise noch Tabak verbrennen, waren von der Analyse ausgeschlossen, ebenso wie Studien, die nicht eine vollständige Abstinenz vom Nikotin zum Ziel hatten.
Primärer Wirksamkeitsendpunkt war eine Abstinenz für 6 Monate und länger; primärer Sicherheitsendpunkt war das Auftreten schwerer Nebenwirkungen, definiert als epileptischer Anfall, Überdosierung, Suizidversuch, Tod, lebensbedrohliche Erkrankung oder längerer stationärer Aufenthalt sowie körperliche Behinderung als Folge der TE. Leichtere, typische Nebenwirkungen einer Entwöhnungstherapie, wie Schlafstörungen, Mundtrockenheit, Übelkeit etc., wurden nicht berücksichtigt. Sekundärer Endpunkt war ein Therapieabbruch bei Unverträglichkeit.
Ergebnisse: Von den 319 RCT kamen die meisten aus USA/Kanada (166) und Europa (82). In 118 Studien wurden finanzielle Zuwendungen durch die Tabak- oder e-Z-Industrie offengelegt. Nur 51 Studien hatten ein als sehr niedrig eingeschätztes Risiko für Bias, 104 ein hohes und 164 ein unklares Risiko. In 22 Studien gab es keinerlei verhaltens- oder psychotherapeutische Unterstützung. 131 RCT wurden nach 6 und 164 nach 12 Monaten beendet; die längste Studie dauerte 5 Jahre; 53 Studien sind derzeit noch nicht abgeschlossen.
Am wirksamsten zur TE waren Ne-Z, Vareniclin und Cytisin: Von 100 Personen stoppten 10-19 das Rauchen mit Hilfe von Ne-Z, 12-16 mit Vareniclin und 10-18 mit Cytisin im Vergleich zu 6 ohne Intervention bzw. mit Plazebo (s. Tab. 1). Unter Kombination von Nikotin-Kaugummi plus Nikotin-Pflaster war die Erfolgsrate durch den additiven Effekt ähnlich hoch wie unter Ne-Z. Nikotin-Pflaster oder -Kaugummi allein sowie Bupropion allein waren weniger erfolgreich, aber immer noch wirksamer als Plazebo. Nortriptylin hatte den geringsten Erfolg. Das Ausschleichen von Nikotin und die Nfe-Z waren nicht wirksamer als Plazebo. Die Evidenz für diese Einschätzung wird als hoch bewertet, und die Ergebnisse änderten sich nicht, wenn die Studien mit hohem Bias-Risiko ausgeklammert wurden.
Therapiesicherheit: Von als schwer definierten Nebenwirkungen waren 3% der Teilnehmer unter Ne-Z, Vareniclin, Cytisin und NRT betroffen (geringe Sicherheit der Evidenz). Dies lag auf dem Niveau von Plazebo; unter Nortriptylin und Nfe-Z lag die Häufigkeit bei 4% mit unsicherer Evidenz. Alle Ergebnisse decken sich mit jüngsten sowie früher publizierten Meta-Analysen [6], [8], [10], [13] [14], [15].
Die Autoren kommen zu dem Schluss, dass nahezu alle Therapien dabei helfen können, über mindestens 6 Monate nicht mehr zu rauchen, und dass sie im Rückblick auf bis zu 50 Jahre überwiegend auch als sicher zu bewerten sind. Sie schlagen Studien vor mit direktem Vergleich der erfolgreichsten Strategien (untereinander und in Kombination) sowie in Kombination mit verhaltenstherapeutischen Maßnahmen.
Ne-Z sind wirksam im akuten Entzug; ob und wie stark das „Vaping“ als vermeintlich „schonenderes Rauchen“ auf lange Sicht negative Folgen hat, kann noch nicht abschließend beurteilt werden. Beim „Vaping“ mit Ne-Z den Nikotinkonsum nicht unkontrolliert zu steigern, bedarf einiger Disziplin; ein Fläschchen „Liquid“ reicht je nach Konsum für 5-10 Tage. Für die nötige Selbstkontrolle besteht dabei eine gewisse Unübersichtlichkeit, denn es entfällt die Maßeinheit „Schachtel Zigarette“. Bei einem eventuellen Rückfall zur Zigarette oder bei Parallelkonsum könnte dann am Ende sogar stärker geraucht werden als zuvor. Aufgrund der bis dahin als unzureichend bewerteten Datenlage und auch wegen der noch nicht abschätzbaren gesundheitlichen Langzeitfolgen, sahen die Autoren der „Nationalen Versorgungsleitlinie COPD“ aus dem Jahre 2021 in der e-Z (noch) keine Option für einen primären Entwöhnungsversuch [16]. Der Einsatz der e-Z soll demnach nur unter bestimmten Voraussetzungen erfolgen: bei dokumentiertem Versagen oder Ablehnung anderer evidenzbasierter Maßnahmen, nach Aufklärung über bekannte Risiken, bei gleichzeitiger Beendigung des Tabakkonsums und bei kontinuierlichem ärztlichem Monitoring und Begleitung. Das zeigt, wie wichtig die Primärprävention ist, z.B. die Aufklärung in Schulen.
Literatur
- Pirie, K., et al. (MWS = Million Women Study): Lancet 2013, 381, 133. (Link zur Quelle)
- “National
- Hartmann-Boyce, J., et al.: Cochrane Database Syst. Rev. 2019, 6, CD009670. (Link zur Quelle)
- AMB 2007, 41, 24b. AMB 2000, 34, 25. (Link zur Quelle)
- S3 Leitlinie Rauchen und Tabakabhängigkeit: Screening, Diagnostik und Behandlung. (Link zur Quelle)
- Livingstone-Banks, J., et al.: Cochrane Database Syst. Rev. 2023, 5, CD006103. (Link zur Quelle)
- Courtney, R.J., et al. (CESSATE = Cytisine versus varEnicline for Smoking cesSATion): JAMA 2021, 326, 56. (Link zur Quelle)
- Hajizadeh, A., et al.: Cochrane Database Syst. Rev. 2023, 5, CD000031. (Link zur Quelle)
- AMB 2007, 41, 36. AMB 2011, 45, 70a. AMB 2015, 49, 46b. (Link zur Quelle)
- Hartmann-Boyce, J., et al.: Cochrane Database Syst. Rev. 2022, 11, CD010216. (Link zur Quelle)
- Warner, K.E., et al.: Nature Medicine 2023, 29, 520. (Link zur Quelle)
- Lindson, N., et al.: Cochrane Database Syst. Rev. 2023, 9, CD015226. (Link zur Quelle)
- Hartmann-Boyce, J., et al.: Cochrane Database Syst. Rev. 2018, 5, CD000146. (Link zur Quelle)
- Theodoulou, A., et al.: Cochrane Database Syst. Rev. 2023, 6, CD013308. (Link zur Quelle)
- Thomas, K.H., et al.: Addiction 2022, 117, 861. (Link zur Quelle)
- S2k-Leitlinie zur Diagnostik und Therapie von Patienten mit chronisch obstruktiver Bronchitis und Lungenemphysem (COPD). (Link zur Quelle)