Zusammenfassung
Ein aktuelles unabhängiges systematisches Review (SR) kommt zu dem Schluss, dass nur Personen mit hohem und sehr hohem Risiko für kardiovaskuläre Ereignisse einen Nutzen von einer antilipidämischen Kombinationsbehandlung mit Statin plus Ezetimib und/oder PCSK9-Hemmer haben. Mit der Kombinationsbehandlung treten weniger nicht-tödliche Myokardinfarkte und Schlaganfälle auf; das Überleben wird nach heutigem Kenntnisstand nicht verlängert. Die absoluten Effekte sind allerdings gering und liegen zwischen 8 und 21 verhinderten „Fällen“ pro 1.000 Personen und 5 Jahren Behandlung. Eine neue Leitlinie zur Zusatzbehandlung mit Ezetimib oder PCSK9-Hemmern zu Statinen basiert auf diesem SR. Sie wendet sich von der Fokussierung auf Lipid-Zielwerte ab und gibt einfache Behandlungsempfehlungen anhand der Höhe des individuellen Risikos. Demnach kommt eine lipidsenkende Kombinationsbehandlung in erster Linie für Personen mit hohem oder sehr hohem Risiko für vaskuläre Erkrankungen in Frage - nach fachlich kompetenter Information in einer gemeinsamen Entscheidung von Arzt und Patient.
Eine Vielzahl von Leitlinien beschäftigt sich mit der medikamentösen Prävention kardiovaskulärer Erkrankungen. Die Empfehlungen hinsichtlich der Therapieziele und des sequenziellen Einsatzes verschiedener Lipidsenker sind trotz gleicher Datenbasis uneinheitlich. Dies ist nach unserer Einschätzung auch Folge der Interessenkonflikte der Autoren, die Leitlinien verfassen bzw. ihrer herausgebenden Institutionen. Diese Verflechtung führt zu großem Misstrauen und Unmut gegenüber diesen Empfehlungen und einer unzureichenden Implementierung in die alltägliche Praxis (vgl. [1]). Es wäre daher wünschenswert, dass Empfehlungen, die so viele Menschen betreffen, einheitlich sind und von Personen und Institutionen erstellt werden, die vertrauenswürdig sind und keine Interessenkonflikte mit den Herstellern von Lipidsenkern haben.
Einigkeit besteht hinsichtlich der medikamentösen Erstlinientherapie. Personen mit erhöhten LDL- bzw. Non-HDL-Cholesterin-Werten, bei denen eine medikamentöse Prävention gewünscht ist, sollten ein Statin einnehmen. Statine senken die Mortalität und nicht-tödliche Herzinfarkte und Schlaganfälle, wobei die absoluten Risikoreduktionen weniger eindrucksvoll sind als die relativen [2]. Unstrittig ist auch, dass der absolute Nutzen einer Statin-Behandlung umso höher ist, je höher das vaskuläre Grundrisiko ist.
Uneinheitlich sind dagegen die Empfehlungen zu den Therapiezielen und wie vorzugehen ist, wenn diese mit Statinen nicht erreicht oder Statine nicht vertragen werden. Nach wie vor gibt es wenig direkte Evidenz aus Interventionsstudien, die verschiedene LDL-Zielwerte miteinander verglichen haben (vgl. [3]) sowie zur Frage, welche Lipidsenker verwendet werden sollen, wenn Statine nicht ausreichen, um diese Ziele zu erreichen oder schlecht vertragen werden. Ezetimib, PCSK9-Hemmer und weitere, neue Wirkstoffe senken zwar das LDL-Cholesterin, die Auswirkungen auf klinische und somit patientenrelevante Endpunkte sind aber teilweise noch nicht bekannt bzw. weniger ausgeprägt als die von Statinen (vgl. [4]). Da alle Zweitlinien-Medikamente teilweise erheblich teurer sind als die Statine, bestehen zudem Zweifel hinsichtlich der Kosteneffektivität [5].
Ein internationales Team, bestehend aus 12 Allgemeinmedizinern, Kardiologen, Internisten, Endokrinologen und Stoffwechselexperten, Geriatern, Public-Health-Experten und Methodikern aus Europa, Nordamerika und China haben Anfang Mai 2022 im British Medical Journal ein Systematisches Review (SR) zum Nutzen von Ezetimib und PCSK9-Hemmern publiziert [6]. In einer Netzwerkanalyse bewerteten sie den Nutzen dieser Wirkstoffe bei Personen mit erhöhtem kardiovaskulärem Risiko, die bereits mit Statinen behandelt werden oder diese nicht vertragen. Das SR wurde ohne Sponsoring erstellt, und die Autoren deklarieren keine Interessenkonflikte.
Methodik: Gesucht wurden randomisierte kontrollierte Studien (RCT) in Medline©, EMBASE©, der Cochrane Library und bei ClinicalTrials.gov, die bis zum 31.12.2020 publiziert waren. Eingeschlossen wurden RCT mit ≥ 500 Probanden und einer Nachbeobachtungszeit von mindestens 6 Monaten. Ausgeschlossen wurden Studien, bei denen im Interventionsarm eine andere Statin-Dosierung verwendet wurde als im Kontrollarm. Außer den monoklonalen Antikörpern bzw. PCSK9-Hemmern Evolocumab und Alirocumab wurden auch Studien zum „small interfering RNA“ (siRNA) Inclisiran eingeschlossen (vgl. [7]). Bempedoinsäure war zum Zeitpunkt des SR noch nicht zugelassen.
Zur Abschätzung des kardiovaskulären Grundrisikos wurde ein noch wenig bekannter Risikorechner mit dem Akronym PREDICT verwendet [8]. In diesen gehen 13 Faktoren ein: Alter, Geschlecht, Ethnie, Raucherstatus, systolischer RR, Behandlung mit Antihypertensiva, Gesamtcholesterin, HDL-Cholesterin, Behandlung mit Lipidsenkern, Familienanamnese für kardiovaskuläre Erkrankungen, Niereninsuffizienz, Vorhofflimmern und schlechter sozioökonomischer Status. PREDICT berechnet das 5-Jahres-Risiko für ein „Major Adverse Cardiac Event“ (MACE): niedriges Risiko (0–5%; Vorliegen von 1-2 Risikofaktoren); moderat erhöhtes Risiko (5-15%; Vorliegen von 3-4 Risikofaktoren); hohes Risiko (15-20%; Vorliegen von ≥ 5 Risikofaktoren oder einer Familiären Hyperlipidämie ohne weitere Risikofaktoren); sehr hohes Risiko (> 20%; manifeste kardiovaskuläre Erkrankung oder Familiäre Hyperlipidämie mit weiteren Risikofaktoren).
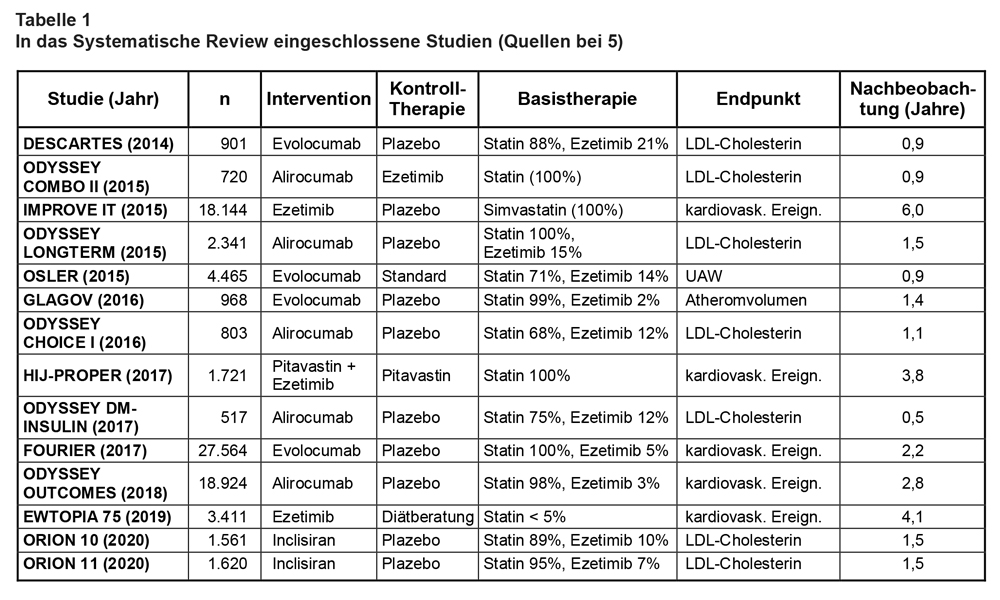
Ergebnisse: Insgesamt wurden 582 Publikationen überprüft und 16 RCT mit insgesamt 111.098 Patienten für das SR ausgewählt. In die Primäranalyse gingen 14 Studien (83.660 Personen) ein. Zwei Studien mit einem nicht zugelassenen PCSK9-Hemmer wurden nur in eine Sensitivitätsanalyse aufgenommen. Drei RCT prüften Ezetimib, 11 einen PCSK9-Hemmer, jeweils zusätzlich zu einer lipidsenkenden Basistherapie, meist ein Statin (s. Tab. 1). Das mediane Alter der Studienteilnehmer betrug 61 Jahre (Interquartilbereich = IQR: 60-65 Jahre), die mediane Nachbeobachtungsdauer 2 Jahre (IQR: 1-3 Jahre). Nur die Hälfte der Studien hatte einen klinischen primären Endpunkt, beispielsweise kardiovaskuläre Ereignisse oder Nebenwirkungen.
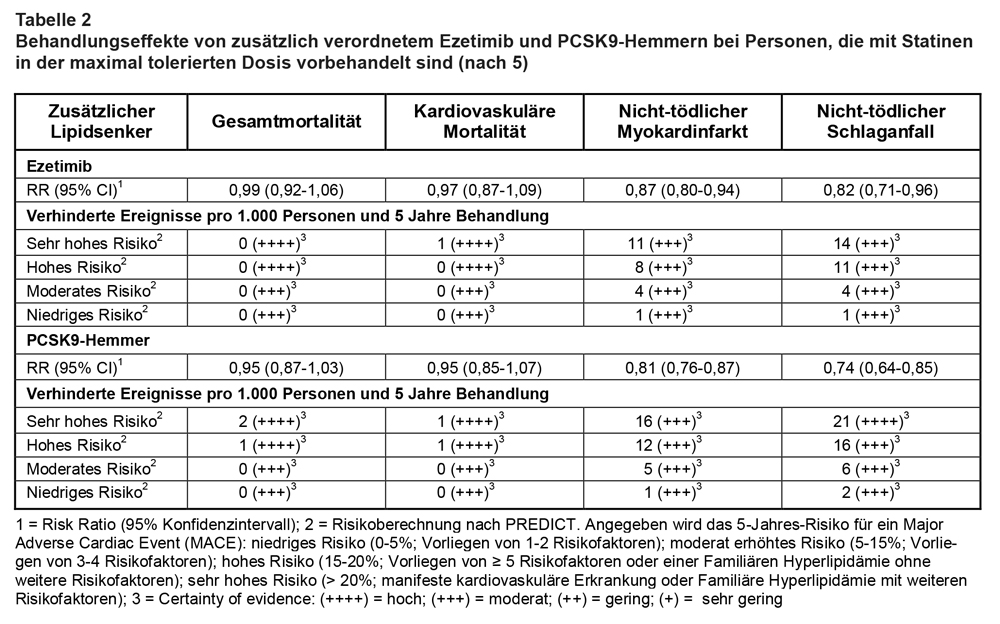
Auswirkungen auf die Gesamt- und kardiovaskuläre Mortalität: Im Vergleich zu den Kontrollgruppen ist weder für Ezetimib noch für PCSK9-Hemmer ein signifikanter additiver Effekt auf die Gesamt- und kardiovaskuläre Mortalität gegenüber einer Statin-Monotherapie in der maximal tolerierten Dosis nachweisbar, auch nicht bei Personen mit sehr hohem kardiovaskulärem Risiko (Tab. 2).
Auswirkungen auf nicht-tödliche Myokardinfarkte und Schlaganfälle: Im Vergleich zu einer Statin-Monotherapie in der maximal tolerierten Dosis ist sowohl mit Ezetimib als auch mit PCSK9-Hemmern ein positiver Effekt auf die Rate nicht-tödlicher Myokardinfarkte und Schlaganfälle nachweisbar, vorrangig bei Personen mit hohem und sehr hohem Grundrisiko. Die absoluten Behandlungseffekte sind klein und bewegen sich im Bereich von 11-21 verhinderten Ereignissen pro 1.000 Personen bei 5-jähriger Therapie. Dies entspricht einer „Number Needed to Treat“ (NNT) von 50-100. PCSK9-Hemmer haben bei Patienten mit hohem und sehr hohem Risiko etwas größere Effekte als Ezetimib (Tab. 2).
Effekte bei Statin-intoleranten Personen: Eine Monotherapie mit Ezetimib hat im Vergleich zu keiner lipidsenkenden medikamentösen Behandlung keinen nachweisbaren Einfluss auf die Gesamtmortalität (Relatives Risiko = RR: 0,99; 95%-Konfidenzintervall = CI: 0,92-1,06) oder die kardiovaskuläre Mortalität (RR: 0,97; CI: 0,87-1,09). Bei Patienten mit sehr hohem und hohem Risiko vermindert Ezetimib nicht-tödliche Herzinfarkte (-16 bzw. -12 pro 1.000 Personen und 5 Jahren Behandlung) und Schlaganfälle (-17 bzw. -13); das entspricht einer „Number needed to treat“ = NNT von 58-76.
Die Monotherapie mit einem PCSK9-Hemmer hat im Vergleich zu keiner lipidsenkenden medikamentösen Behandlung ebenfalls keinen nachweisbaren Einfluss auf die Gesamtmortalität (RR: 0,95; CI: 0,87-1,03) und die kardiovaskuläre Mortalität (RR: 0,95; CI: 0,85-1,07). PCSK9-Hemmer reduzieren bei Patienten mit sehr hohem und hohem Risiko nicht-tödliche Herzinfarkte (-23 bzw. -17 pro 1.000 Personen und 5 Jahren Behandlung) und Schlaganfälle (-24 bzw. -18); das entspricht einer NNT von 42-59. PCSK9-Hemmer scheinen also etwas wirksamer zu sein als Ezetimib.
Auch die Kombinationsbehandlung PCSK9-Hemmer plus Ezetimib senkt gegenüber keiner Behandlung wahrscheinlich nicht das Mortalitätsrisiko. Gegenüber einer Monotherapie mit einem der beiden Wirkstoffe sinkt jedoch das Risiko für nicht-tödliche Herzinfarkte und Schlaganfälle um weitere 13-20 „Fälle“ pro 1.000 Personen und 5 Jahren Behandlung.
Als wesentliche Einschränkungen der Ergebnisse ihres SR nennen die Autoren, dass es keine direkten Vergleiche zwischen den untersuchten Lipidsenkern gibt und dass daher die Evidenz nur indirekt ist. Außerdem konnten wegen fehlendem Zugriff auf die Rohdaten der Studien keine vertiefenden Analysen erfolgen, z.B. hinsichtlich der Effekte bei hohem oder niedrigem Lebensalter, der Nachbeobachtungs- bzw. Behandlungsdauer oder verschiedenen Ausgangswerten des LDL-Cholesterins. Derartige differenzierte Betrachtungen wären wünschenswert.
Neue Empfehlungen: Basierend auf diesem SR veröffentlicht in der gleichen Ausgabe des British Medical Journal eine interdisziplinäre Expertengruppe um den Allgemeinmediziner Nicolas Delvaux vom Department of Public Health and Primary Care aus Leuven in Belgien als „BMJ Rapid Recommendation“ eine „Clinical Practice Guideline“ zur Anwendung von Ezetimib und PCSK9-Hemmern [9]. Diese fügt sich in ein neues Leitlinienprogramm mit dem Akronym MAGIC ein („Making GRADE the Irresistible Choice“), welches während der COVID-19-Pandemie vom British Medical Journal und der norwegischen „MAGIC Evidence Ecosystem Foundation“ ins Leben gerufen wurde, um auf den raschen Wissenszuwachs während der Pandemie zu reagieren und den Anwendern „vertrauenswürdige“ und im klinischen Alltag hilfreiche Empfehlungen zu geben [10]. MAGIC bietet einen neuen Ansatz zur Erstellung und Verbreitung von Leitlinien und soll dabei helfen, die vielen Mängel in der gegenwärtigen Praxis zu beseitigen, wie beispielsweise intransparente Verfahren, mangelnde Unabhängigkeit der Autoren, schlechte Lesbarkeit, fehlende Aktualisierungen oder Scheitern bei der Implementierung in der alltäglichen Praxis. Wir haben diese Punkte in der Vergangenheit häufig kritisiert (vgl. [11]). Dabei wird ein neues, webbasiertes Instrument angewendet (MAGICapp), das Autoren, Organisationen und Anwender interaktiv dabei unterstützt, Leitlinien strukturiert zu erstellen, zu diskutieren, in benutzerfreundlichen Formaten zu veröffentlichen und das Wissen fortlaufend zu aktualisieren.
Die neuen Empfehlungen zu Ezetimib und PCSK9-Hemmern stammen von 27 Autoren aus 5 Kontinenten. Darunter sind Allgemeinmediziner, Internisten, Kardiologen, Endokrinologen, Geriater, Methodiker und auch drei Patientenvertreter. Niemand aus dem Gremium gibt finanzielle Interessenkonflikte an. Die Empfehlungen gelten für erwachsene Patienten, die zur Prävention eines kardiovaskulären Ereignisses mit einem Statin behandelt werden und noch ein LDL-Cholesterin > 70 mg/dl haben, oder die kein Statin vertragen. Andere Zielwerte werden nicht genannt. Die neue Leitlinie wendet sich explizit von der Fokussierung auf Lipid-Zielwerte ab. Es soll also kein Laborwert behandelt, sondern das individuelle kardiovaskuläre Risiko gesenkt werden. Dieses soll mit Hilfe „vertrauenswürdiger Risikorechner“ identifiziert und die Behandlung im Rahmen einer guten fachlichen Information und gemeinsamen Entscheidung erfolgen. Solch ein Vorgehen sei besonders wichtig, wenn die Beweislage schwach ist.
Die Empfehlungen sind einfach und klar (Tab. 3) und beinhalten erklärende Darstellungen der „certainty of evidence“ (nach GRADE; [12]) sowie Informationen zu möglichen Nebenwirkungen bzw. der Nutzen-Risiko-Relation. Dabei wird auch erwähnt, dass zur Langzeit-Sicherheit von PCSK9-Hemmern nach wie vor wenig bekannt ist. Als Ergänzung sollten künftig die Definitionen von „familiärer Hyperlipidämie“ (heterozygot, homozygot, positive Familienanamnese für frühen Herzinfarkt oder Schlaganfall) und „manifester kardiovaskulärer Erkrankung“ noch präziser formuliert werden: zählt beispielsweise bereits der Nachweis eines Plaques in der Bildgebung oder muss ein klinisches Ereignis vorliegen?
Literatur
- AMB 2019, 53, 73. AMB 2020, 54, 65. (Link zur Quelle)
- Byrne, P., et al.: JAMA Intern. Med. 2022, 182, 474. https://jamanetwork.com/journals/jamainternalmedicine/article-abstract/2790055 (Link zur Quelle)
- AMB 2020, 54, 05. (Link zur Quelle)
- AMB 2015, 49, 04. AMB 2018, 52, 91. AMB 2021, 55, 97. AMB 2022, 56, 05. (Link zur Quelle)
- Marquina, C., et al.: Pharmacoeconomics 2020, 38, 1095. https://link.springer.com/article/10.1007/s40273-020-00936-0 (Link zur Quelle)
- Khan, S.U., et al.: BMJ 2022, 377, e069116. https://www.bmj.com/content/377/bmj-2021-069116?msclkid=f195a016cf7c11ec846e9d7bc491ac39 (Link zur Quelle)
- AMB 2021, 55, 97. (Link zur Quelle)
- Pylypchuk, R., et al. (PREDICT = PREDICT Cardiovascular Disease Cohort in New Zealand Primary Care): Lancet 2018, 391, 1897. https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(18)30664-0/fulltext (Link zur Quelle)
- Hao, Q., et al.: BMJ 2022, 377, e069066. https://www.bmj.com/content/377/bmj-2021-069066.long (Link zur Quelle)
- https://magicevidence.org/ (Zugriff am 8.5.2022). (Link zur Quelle)
- AMB 2013, 47, 24DB01. AMB 2019, 53, 08DB01. AMB 2019, 53, 32. AMB 2021, 55, 43b. (Link zur Quelle)
- https://bestpractice.bmj.com/info/toolkit/learn-ebm/what-is-grade/ (Link zur Quelle)